题目内容
25℃时,某硫酸铜溶液的质量分数为w,物质的量浓度为c mol?L-1,密度为ρ g?mL-1,将此溶液蒸去a g水或再向原溶液中加入b g无水硫酸铜粉末,充分静置并恢复至25℃时,均恰好全部转化为CuSO4?5H2O晶体.则下列关系式正确的是
- A.c=
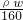
- B.w=
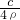
- C.16a=9b
- D.9a=16b
C
分析:A、物质的量浓度C= 判断;
判断;
B、w=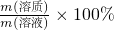 判断;
判断;
C、b g无水硫酸铜的物质的量和a g水的物质的量之比为1:5;
D、b g无水硫酸铜的物质的量和a g水的物质的量之比为1:5.
解答:A、C= =
= =
=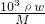 =
=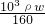 mol/L,故A错误;
mol/L,故A错误;
B、w=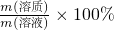 =
=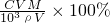 =
=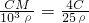 ,故B错误;
,故B错误;
C、根据题意知,b g无水硫酸铜和a g水恰好能形成五水硫酸铜,即b g无水硫酸铜的物质的量和ag水的物质的量之比为1:5,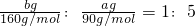 ,所以16a=9b,故C正确;
,所以16a=9b,故C正确;
D、根据题意知,b g无水硫酸铜和a g水恰好能形成五水硫酸铜,即b g无水硫酸铜的物质的量和ag水的物质的量之比为1:5,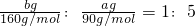 ,所以16a=9b,故D错误;
,所以16a=9b,故D错误;
故选C.
点评:本题考查了各物理量之间的关系,注意计算过程中ρV和CV中溶液的体积单位不同,否则会导致错误.
分析:A、物质的量浓度C=
 判断;
判断;B、w=
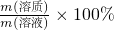 判断;
判断;C、b g无水硫酸铜的物质的量和a g水的物质的量之比为1:5;
D、b g无水硫酸铜的物质的量和a g水的物质的量之比为1:5.
解答:A、C=
 =
= =
=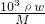 =
=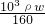 mol/L,故A错误;
mol/L,故A错误;B、w=
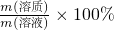 =
=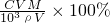 =
=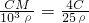 ,故B错误;
,故B错误;C、根据题意知,b g无水硫酸铜和a g水恰好能形成五水硫酸铜,即b g无水硫酸铜的物质的量和ag水的物质的量之比为1:5,
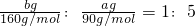 ,所以16a=9b,故C正确;
,所以16a=9b,故C正确;D、根据题意知,b g无水硫酸铜和a g水恰好能形成五水硫酸铜,即b g无水硫酸铜的物质的量和ag水的物质的量之比为1:5,
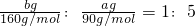 ,所以16a=9b,故D错误;
,所以16a=9b,故D错误;故选C.
点评:本题考查了各物理量之间的关系,注意计算过程中ρV和CV中溶液的体积单位不同,否则会导致错误.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
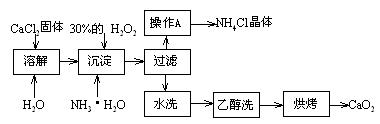
信息时代给人们的生活带来了极大的便利,但同时也产生了大量的电子垃圾.某化学兴趣小组将一批废弃的线路板简单处理后,得到了主要含Cu、Al及少量Fe、Au等金属的混合物,并设计了如下制备硫酸铜晶体和硫酸铝晶体的路线:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Cu(OH)2 |
| 开始沉淀 | 1.1 | 4.0 | 5.4 |
| 完全沉淀 | 3.2 | 5.2 | 6.7 |

(1)过滤操作中用到的玻璃仪器有______.
(2)Cu可溶于稀硫酸与H2O2的混合溶液,其离子方程式是______.
(3)滤渣a的主要成分是______.
(4)步骤③中X的取值范围是______.
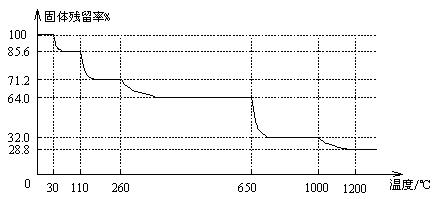
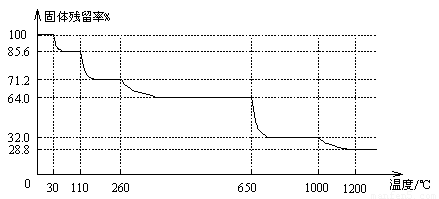
(5)假设制得的CuSO4?5H2O中只含Na2SO4杂质,若用该样品进行“硫酸铜晶体结晶水含量的测定”实验,测得结晶水含量______(填“偏低”、“偏高”或“无影响”).乙同学取1.280g该样品,加热至恒重称得质量变为0.830g,则此样品的纯度为______.(用小数表示,保留三位有效数字)