题目内容
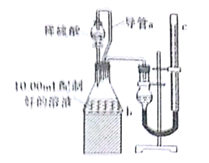
【题目】为了测定某氯酸钾与二氧化锰混合物中氯酸钾的质量分数,课外小组的同学设计了如下实验:取3.0g 混合样品放入如图所示的大试管中,充分加热,直到反应完全,并用如图所示装置测量出生成氧气的体积。试回答下列问题:
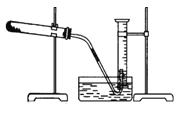
(1)如何检查装置的气密性?
(1)现有如下可供选择的操作:①将导气管放入盛满水的量筒内;②给药品加热;③有连续气泡产生时开始收集气体;④取出导气管;⑤反应完全后停止加热(如图,此时导管出口略高于液面);⑥冷却至室温;⑦调整量筒内外液面高度使之相同后读出量筒内气体体积数。
为了较准确地测量出生成的氧气在常温、常压下的体积,正确的操作顺序是(填序号)______________。
(3)为了较准确地测量到气体的体积,需要调整量筒内外液面高度,其原理是:____________________。
(4)在常温常压下共收集到气体680mL(此时氧气密度为1.41g·L-1),其质量为_______g,原混合物中氯酸钾的质量分数约是______________。
【答案】(1)将导管出口浸入水槽的水中,手握住试管,有气泡逸出,松开手后有少量水进入导管,表明装置不漏气。
(2)①②③⑤⑥⑦④
(3)保证量筒内外气压相等。
(4)0.96g;81.7%
【解析】
试题分析:(1)检验装置的气密性:将导管出口浸入水槽的水中,手握住试管或者用热毛巾握住试管,有气泡逸出,松开手后有少量水进入导管,表明装置不漏气;(2)正确的实验操作顺序,要注意先加热、后熄灯,等有连续气泡产生时再开始收集气体,具体顺序为:①②③⑤⑥⑦④;(3)只有量筒内外液面高度相等时,量筒内外气压才相等,所以需要调整量筒内外液面高度;(4)由密度公式:m(O2)=1.41gL-1x0.680L=0.96g;再由制取氧气的化学方程式:
2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
245 96
x 0.96 解得:x=2.45g
原混合物中氯酸钾的质量分数约:2.45g/3.0g=81.7%

 阅读快车系列答案
阅读快车系列答案