题目内容
12.下列各组物质的类别归属正确的是( )| A. | 同位素:1H2、2H2、3H2 | B. | 分子晶体:I2、SO3、固态氩 | ||
| C. | 非电解质:Cl2、BaSO4、C2H5OH | D. | 化合物:重水、双氧水、矿泉水 |
分析 A.有相同质子数,不同中子数的原子或同一元素的不同核素互为同位素;
B.分子晶体:分子间通过分子分子间作用力(包括范德华力和氢键)构成的晶体;
C.非电解质:在熔融状态和水溶液中都不能导电的化合物;
D.化合物:由两种或两种以上的元素组成的纯净物.
解答 解:A.1H2、2H2、3H2是由氢的不同核素形成的单质,故A错误;
B.I2、SO3、固态氩都是分子晶体,故B正确;
C.Cl2是单质,既不是电解质,也不是非电解质,BaSO4是强电解质,C2H5OH是非电解质,故C错误;
D.重水和双氧水都是化合物,矿泉水是混合物,故D错误,
故选B.
点评 本题考查同位素、化合物、非电解质和分子晶体的概念,难度不大,要注意平时知识的积累,明确相关的概念是解题的关键.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
7.钼可用于制导弹,钼的同位素${\;}_{42}^{94}$Mo所含的中子数是( )
| A. | 42 | B. | 47 | C. | 52 | D. | 94 |
17.某无色透明溶液中可能大量存在Ag+,Mg2+,Cu2+中的几种离子.
①取少量原溶液加入过量稀盐酸,有白色沉淀生成,再加过量稀硝酸,白色沉淀不消失.
②在上述①溶液的滤液中加入过量NaOH溶液,出现白色沉淀.
则原溶液中可能大量存在的阴离子是( )
①取少量原溶液加入过量稀盐酸,有白色沉淀生成,再加过量稀硝酸,白色沉淀不消失.
②在上述①溶液的滤液中加入过量NaOH溶液,出现白色沉淀.
则原溶液中可能大量存在的阴离子是( )
| A. | Cl- | B. | NO3- | C. | CO32- | D. | OH- |
2.下列离子检验的正确的是( )
| A. | 某酸性溶液中滴入氯化钡溶液,生成白色沉淀,说明原溶液中一定有SO42- | |
| B. | 某酸性溶液中滴入硝酸银溶液,生成白色沉淀,说明原溶液中一定有Cl- | |
| C. | 某溶液中滴入稀盐酸,生成无色气体,说明原溶液中有一定有CO32- | |
| D. | 某溶液中滴入氢氧化钠溶液,生成蓝色沉淀,说明原溶液中一定有Cu2+ |
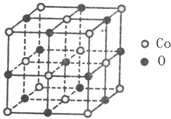 我国为钴(Co)消费大国,以化合物形式消费的钴主要用作催化剂、磁性材料、电池材料、超硬材料、干燥剂、颜料与染料等领域.
我国为钴(Co)消费大国,以化合物形式消费的钴主要用作催化剂、磁性材料、电池材料、超硬材料、干燥剂、颜料与染料等领域.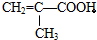 则:
则: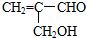 ;
;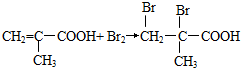 .
.