题目内容
【题目】I.金属矿物资源以及海水资源的利用有着非常重要的意义。
Ⅰ(1)金属铁常用的冶炼方法是____________(填序号);
A.热分解法 B.热还原法 C.电解法 D.湿法冶金
(2)利用冶炼得到的铁屑和海带中提取的碘可以用于生产KI,其工艺流程如图所示:
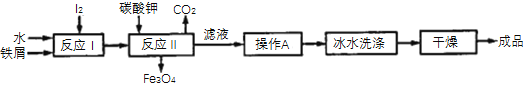
①操作A包括________________、_____________、过滤。
②用冰水洗涤的目的是:a除去附着在KI表面的可溶性杂质:b._________________。
③反应Ⅰ生成了铁与碘的化合物X,若X中铁元素与碘元素的质量比为21∶127,则X的化学式为__________________;反应Ⅱ中1molX完全反应生成89.6L(标准状况)CO2,写出反应Ⅱ的化学方程式:______________________________________________。
Ⅱ.工业上由黄铜矿(主要成分CuFeS2)冶炼铜的主要流程如下:
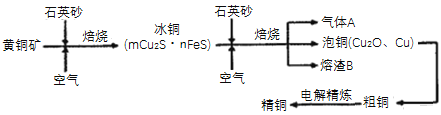
(3)气体A中的大气污染物可选用下列试剂中的____________吸收。
a.浓HSO4 b.稀HNO3 c.NaOH溶液 d.氨水
(4)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在_____(填离子符号),检验溶液中还存在Fe2+的方案是:____________________________。
(5)在一定量的精铜中加入足量的稀HNO3溶液,该反应的离子方程式为________________。
(6)由泡铜冶炼粗铜的化学反应方程式为______________________________________。
【答案】B 加热浓缩 冷却结晶 同时减少KI的溶解损失 Fe3I8 Fe3I8+4K2CO3=Fe3O4+8KI+4CO2↑ c d Fe3+ 取少量溶液,滴加KMnO4溶液,KMnO4褪色 3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O 3Cu2O+2Al![]() Al2O3+6Cu
Al2O3+6Cu
【解析】
Ⅰ(1)金属的冶炼一般有电解法、热还原法、热分解法、物理分离法。电解法:冶炼活泼金属K、Ca、Na、Mg、Al,一般用电解熔融的氯化物(Al是电解熔融的三氧化二铝)制得;热还原法:冶炼较不活泼的金属Zn、Fe、Sn、Pb、Cu,常用还原剂有(C、CO、H2等);热分解法:Hg、Ag用加热分解氧化物的方法制得,物理分离法:Pt、Au用物理分离的方法制得;
(2)①得到碘化钾,需要经过加热浓缩、冷却结晶、过滤,再降温、干燥得到碘化钾固体;
②冰水洗涤的目的是:洗涤除去表面可溶性杂质,同时减少KI的溶解损失;
③铁元素与碘元素的质量比为21:127,铁、碘原子个数比为3:8,反应Ⅰ生成了Fe3I8,反应中Ⅱ1mol X完全反应生成89.6L(标准状况)CO2,据此根据得失电子守恒可知,书写反应Ⅱ的化学反应方程式;
Ⅱ由流程可知,黄铜矿加入石英砂通入空气焙烧,可生成Cu2S、CuO,继续加入石英砂通入空气焙烧,生成Cu2O、Cu,生成气体A为二氧化硫,熔渣B为FeO等,Cu2O、Cu与铝在高温下发生铝热反应得到粗铜,电解可得到精铜,根据分析解答。
Ⅰ(1)A.冶炼不活泼的金属,用热分解法,如Hg、Ag用加热分解氧化物的方法制得,故A错误;
B.热还原法冶炼较不活泼的金属Fe、Cu,常用还原剂有(C、CO、H2等),故B正确;
C.电解法冶炼活泼金属Na、Al,一般用电解熔融的氯化物(Al是电解熔融的三氧化二铝)制得,故C错误;
D.湿法冶金用较活泼的金属从溶液中置换出活泼性相对弱的金属,如我国古代利用铁和硫酸铜溶液反应炼铜,反应为Fe+CuSO4=Cu+FeSO4,属于湿法冶金,故D错误;
故答案为:B;
(2)①反应Ⅱ的滤液需要经过加热浓缩、冷却结晶、过滤,初步得到碘化钾;
②冰水晶体溶解度小,由于碘化钾混有可溶性杂质,需要经过洗涤才能得到较纯净的产品,故用冰水洗涤,洗涤除去表面可溶性杂质,同时减少KI的溶解损失;
③铁元素与碘元素的质量比为21:127,铁、碘原子个数比为![]() :
:![]() =3:8,反应Ⅰ生成了Fe3I8,反应中Ⅱ1molX完全反应生成89.6L(标准状况)CO2,生成二氧化碳气体的物质的量为
=3:8,反应Ⅰ生成了Fe3I8,反应中Ⅱ1molX完全反应生成89.6L(标准状况)CO2,生成二氧化碳气体的物质的量为![]() =4mol,所以反应Ⅱ是Fe3I8和碳酸钾反应生成四氧化三铁、二氧化碳与KI,反应Ⅱ的反应方程式是:Fe3I8+4K2CO3=Fe3O4+8KI+4CO2↑;
=4mol,所以反应Ⅱ是Fe3I8和碳酸钾反应生成四氧化三铁、二氧化碳与KI,反应Ⅱ的反应方程式是:Fe3I8+4K2CO3=Fe3O4+8KI+4CO2↑;
Ⅱ(3) 由流程图转化可知,气体A中的大气污染物主要是二氧化硫,选择试剂吸收二氧化硫,不能产生新的污染气体,
a.浓H2SO4不能吸收二氧化硫,故a错误;
b.稀HNO3可以吸收二氧化硫,但生成NO污染大气,故b错误;
c.NaOH溶液与二氧化硫反应生成亚硫酸钠,故c正确;
d.氨水与二氧化硫反应生成亚硫酸铵,故d正确;
故选cd;
(4)用稀H2SO4浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明含有Fe3+;Fe2+具有还原性,可以利用KMnO4溶液检验,取少量溶液,滴加KMnO4溶液,KMnO4溶液紫色褪去;
(5)铜和稀硝酸反应生成硝酸铜、一氧化氮和水,反应的离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
(6)由流程图转化可知,Cu2O与Al反应置换反应生成Al2O3与Cu,反应方程式为3Cu2O+2Al![]() Al2O3span>+6Cu。
Al2O3span>+6Cu。

【题目】实验室用下图装置完成表中的四个实验,不能达到实验目的的是
实验装置 | 实验目的 | 试剂X | 试剂Y | |
| A. | 检验C2H5Br消去反应后的气体产物 | 水 | 酸性KMnO4溶液 |
B. | 检验C2H5OH消去反应后的气体产物 | NaOH溶液 | Br2的CCl4溶液 | |
C. | 比较醋酸、碳酸、苯酚酸性强弱 | NaOH溶液 | 苯酚钠溶液 | |
D. | 检验制取乙炔时的气体产物 | CuSO4溶液 | 酸性KMnO4溶液 |
A. AB. BC. CD. D