题目内容
16.在四个不同的容器中,进行2A(g)+3B(g)?4C(g)+D(g)反应.根据在相同时间内测定的结果判断,生成C的速率最快的是( )| A. | v(A)=0.3mol.L-1.min-1 | B. | v(B)=0.4 mol.L-1.min-1 | ||
| C. | v(C)=0.7 mol.L-1.min-1 | D. | v(D)=0.2 mol.L-1.min-1 |
分析 不同物质表示的反应速率之比等于其化学计量数之比,故不同物质表示的速率与其化学计量数的比值越大,表示的反应速率越快,注意保持单位一致.
解答 解:A.$\frac{v(A)}{2}$=0.15mol•L-1•min-1;
B.$\frac{v(B)}{3}$=0.133mol•L-1•min-1;
C.$\frac{v(C)}{4}$=0.175mol•L-1•min-1;
D.$\frac{v(D)}{1}$=0.2mol•L-1•min-1,
故反应速率v(D)>v(C)>v(A)>v(B)
故选D.
点评 本题考查化学反应速率快慢比较,比较基础,利用比值法可以迅速判断,也可以转化为同一物质表示的速率进行比较,注意单位保持一致.

练习册系列答案
相关题目
6.花生油和柴油虽然都被称作“油”,但从化学组成和分子结构来看,它们是完全不同的.下列说法中正确的是( )
| A. | 花生油属于纯净物,柴油属于混合物 | |
| B. | 花生油属于酯类,柴油属于烃类 | |
| C. | 花生油属于有机物,柴油属于无机物 | |
| D. | 花生油属于高分子化合物,柴油属于小分子化合物 |
7.可逆反应2SO2(g)+O2(g)?2SO3(g)在恒容密闭容器中达到平衡,下列说法正确的是( )
| A. | SO2和O2不再化合,反应停止了 | |
| B. | 容器内压强保持不变 | |
| C. | SO2、O2和 SO3的浓度相等 | |
| D. | SO2、O2和 SO3的物质的量之比为2:1:2 |
4.现有7瓶失去标签的液体,已知它们是有机试剂,可能是:①乙醇、②乙酸、③苯、④乙酸乙酯、⑤油脂、⑥葡萄糖溶液、⑦蔗糖溶液,现通过如下实验来确定各试剂瓶中所装的液体:
试给它们的试剂瓶重新贴上标签,其中:
A乙醇,C苯,E油脂,F葡萄糖,G蔗糖溶液.
| 实验步骤和方法 | 实验现象 |
| ①把7瓶液体分别依次标号A?B?C?D?E?F?G后,闻气味 | 只有F?G两种液体没有气味 |
| ②各取少量于试管中加水稀释 | 只有C?E?D三种液体不溶解而浮在水面上 |
| ③分别取少量7种液体于试管中加新 制Cu(OH)2悬浊液并加热 | 只有B使沉淀溶解,F中产生砖红色沉淀 |
| ④各取少量C?E?D于试管中,加稀NaOH 溶液并加热 | 只有C仍有分层现象,且在D的试管中闻 到特殊香味 |
A乙醇,C苯,E油脂,F葡萄糖,G蔗糖溶液.
11.丙烯酸的结构简式为CH2=CH-COOH,下列说法不正确的是( )
| A. | 与钠反应放出氢气 | B. | 能与新制的Cu(OH)2悬浊液反应 | ||
| C. | 能与新制银氨溶液发生银镜反应 | D. | 能发生加聚反应生成高分子化合物 |
1.试剂B、C分别是( )
| A. | NaOH、CuSO4 | B. | NaOH、新制Cu(OH)2 | C. | Na2CO3、CuSO4 | D. | H2SO4、新制Cu(OH)2 |
8.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4 L己烷中的分子数约为NA个 | |
| B. | 常温常压下,在18 g H218O中含有NA个水分子 | |
| C. | 标准状况下,15 g CH3CH3所含共价键数为3.5NA个 | |
| D. | 电解精炼铜时,若电路中转移的电子数为2NA个,则阳极质量减轻64 g |
5.如图是某可逆反应在反应过程中的各物质的物质的量(v)与时间(t)的关系曲线.下列叙述正确的是( )
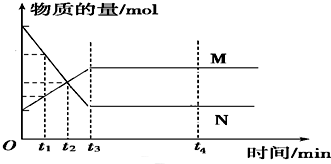

| A. | t1~t2时,只有正方向反应 | B. | t3~t4,反应不再发生 | ||
| C. | t3时,反应达到平衡 | D. | t3~t4,各物质的浓度相等 |
6.银锌电池广泛用于各种电子仪器,电池反应:Ag2O+Zn+H2O$?_{充电}^{放电}$2Ag+Zn(OH)2,下列说法正确的是( )
| A. | 电池在放电时,Ag电极是电池的负极 | |
| B. | 充电时阳极发生的电极反应是:2Ag+2OH--2e-═Ag2O+H2O | |
| C. | 该电池可用酸作电解质溶液 | |
| D. | 充电时电流从Zn电极经电解质溶液流向外接电源的正极 |