题目内容
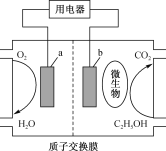
【题目】乙醇做为可再生能源比化石能源具有较大的优势,如图为乙醇燃料电池,该电池的总反应方程式为C2H5OH+3O2=2CO2+3H2O。下列关于该电池叙述错误的是
A.a极与用电器的正极相接B.该装置将化学能转化为电能
C.质子(H+)由装置左侧向右侧移动D.该装置的电解质溶液呈酸性
【答案】C
【解析】
由题干中原电池的总反应方程式C2H5OH+3O2=2CO2+3H2O可知,O2中氧元素的化合价降低,O2在正极得电子,碳元素的化合价升高,乙醇在负极失电子。
A.由图示可知,a极通入O2,则a极为原电池的正极,应与用电器的正极相接,A正确;
B.该装置为乙醇燃料电池,属于原电池装置,将化学能转化为电能, B正确;
C.在原电池中,阳离子移向正极,质子由装置右侧向左侧移动,C错误;
D.该装置中的交换膜为质子交换膜,说明电解质溶液呈酸性,D正确;
故选C。

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目