题目内容
【题目】下列叙述正确的是( )
A.破坏乙烯分子里![]() 所需吸收的能量是破坏乙烷分子里 C—C 能量的两倍
所需吸收的能量是破坏乙烷分子里 C—C 能量的两倍
B.乙烯分子和苯分子都能使溴水褪色,两者褪色原理相同
C.因为甲烷和苯都不能被酸性 KMnO4 溶液氧化,所以两者都不能发生氧化反应
D.甲烷和苯都能和氯气发生取代反应,但是两者发生反应时需要的条件不同
【答案】D
【解析】
A.破坏乙烯分子里![]() 所需吸收的能量小于破坏乙烷分子里C—C能量的两倍,A选项错误;
所需吸收的能量小于破坏乙烷分子里C—C能量的两倍,A选项错误;
B.乙烯可与溴水中的溴发生加成反应使其褪色,苯能够萃取溴水中的溴使其褪色,两者褪色原理不相同,B选项错误;
C.甲烷和苯可以在空气中燃烧,两者的燃烧反应是氧化还原反应,C选项错误;
D.甲烷和氯气在光照条件下发生取代反应,苯和氯气在Fe3+催化的作用下发生取代反应生成氯苯,两者发生发应的条件不同,D选项正确;
答案选D。

 阅读快车系列答案
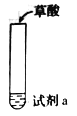
阅读快车系列答案【题目】探究草酸(H2C2O4)性质,进行如下实验。(已知:室温下,0.1 mol·L1 H2C2O4的pH=1.3)
实验 | 装置 | 试剂a | 现象 |
① |
| Ca(OH)2溶液(含酚酞) | 溶液褪色,产生白色沉淀 |
② | 少量NaHCO3溶液 | 产生气泡 | |
③ | 酸性KMnO4溶液 | 紫色溶液褪色 | |
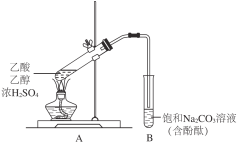
④ | C2H5OH和浓硫酸 | 加热后产生有香味物质 |
由上述实验所得草酸性质所对应的方程式不正确的是
A. H2C2O4有酸性,Ca(OH)2+ H2C2O4![]() CaC2O4↓+2H2O
CaC2O4↓+2H2O
B. 酸性:H2C2O4> H2CO3,NaHCO3+ H2C2O4![]() NaHC2O4+CO2↑+H2O
NaHC2O4+CO2↑+H2O
C. H2C2O4具有还原性,2![]() +5
+5![]() +16H+
+16H+![]() 2Mn2++10CO2↑+ 8H2O
2Mn2++10CO2↑+ 8H2O
D. H2C2O4可发生酯化反应,HOOCCOOH+2C2H5OH![]() C2H5OOCCOOC2H5+2H2O
C2H5OOCCOOC2H5+2H2O
【题目】亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃)是一种黄色气体,遇水易水解。可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
(1)甲组的同学拟制备原料气NO和Cl2,制备装置如下图所示:

为制备纯净干燥的气体,下表中缺少的药品是:
装置Ⅰ | 装置Ⅱ | ||
烧瓶中 | 分液漏斗中 | ||
制备纯净Cl2 | MnO2 | ①___ | ②___ |
制备纯净NO | Cu | ③___ | ④___ |
(2)乙组同学利用甲组制得的NO和Cl2制备NOCl,装置如图所示:
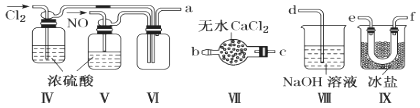
①装置连接顺序为a→________(按气流自左向右方向,用小写字母表示)。
②装置Ⅳ、Ⅴ除可进一步干燥NO、Cl2外,另一个作用是____________。
③装置Ⅶ的作用是____________。
④装置Ⅷ中吸收尾气时,NOCl发生反应的化学方程式为________________。
(3)丙组同学查阅资料,查得王水是浓硝酸与浓盐酸的混酸,一定条件下该混酸可生成亚硝酰氯和氯气, 该反应的化学方程式为__________________。