题目内容
下图为番茄电池,下列说法正确的是( )


| A.一段时间后,锌片质量会变小 | B.铜电极附近会出现蓝色 |
| C.番茄中的阴离子移向铜 | D.锌电极是该电池的正极 |
A
试题分析:该电池为原电池,Zn片为作为负极,发生如下反应:
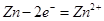 ,通电一段时间后,锌片质量会变小 ,
,通电一段时间后,锌片质量会变小 ,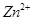 向正极方向移动,而阴离子向负极移动,
向正极方向移动,而阴离子向负极移动, ,铜电极附近应该会出现经砖红色,而不是蓝色,综上可知只有A项正确。
,铜电极附近应该会出现经砖红色,而不是蓝色,综上可知只有A项正确。点评:原电池是高一必修2中的重点也是难点,本题考查学生对于原电池原理的掌握情况,培养学生分析问题的能力。

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
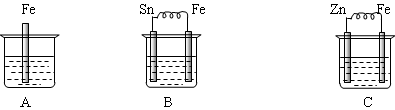



 以上是以NO形式存在的,可发生反应NO(g)+ O3 (g)
以上是以NO形式存在的,可发生反应NO(g)+ O3 (g)  NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如下图)所示。由图可得出的正确说法是
NO2(g)+ O2 (g)。在一定条件下,将NO和O3通入绝热恒容密闭容器中发生上述反应 ,正反应速率随时间变化的示意图(如下图)所示。由图可得出的正确说法是 
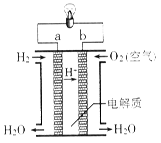
 2H2O
2H2O