题目内容
5.常温下,下列试剂的保存方法不正确的是( )| A. | 氢氟酸保存于棕色玻璃瓶中 | B. | 新制的氯水保存于棕色玻璃瓶中 | ||
| C. | 实验室少量的钠保存于煤油中 | D. | 浓硝酸运输时保存在铝制容器中 |
分析 化学试剂的存放与化学试剂的物理性质和化学性质有关,易挥发的物质要密封保存,见光易分解的物质要避光保存,易与氧气、水、二氧化碳反应的物质要隔绝空气保存,以此解答该题.
解答 解:A.氢氟酸会与玻璃发生反应生成水和四氟化硅,不能贮存在细口玻璃瓶里,应放在塑料瓶中,故A错误;
B.氯水中的次氯酸见光易分解而导致Cl2水变质,应于棕色试剂瓶避光保存,故B正确;
C.钠易与水和氧气反应,所以要隔绝空气保存,钠的密度大于煤油的,且和煤油不反应,所以可用煤油保存,故C正确;
D.浓硝酸见光易分解,所以应避光保存,应保存在棕色试剂瓶中,故D正确.
故选A.
点评 本题考查化学试剂的存放,题目难度不大,注意物质的性质影响保存方法的选择.

练习册系列答案
相关题目
16.下列关于金属钠及化合物的叙述错误的是( )
| A. | 金属钠着火时,可用泡沫灭火器来灭火 | |
| B. | Na2O2与水及CO2反应产生等量O2时,转移电子数相等 | |
| C. | 钠与熔融的四氯化钛反应可制取钛 | |
| D. | 不可用石灰水区分Na2CO3与NaHCO3溶液 |
13.下列说法正确的是(NA 代表阿伏加德罗常数的值)( )
| A. | 17g 氨气含有的原子总数为NA | |
| B. | 2.4 g 金属镁与氧气完全反应时失去电子总数为NA | |
| C. | 常温常压下,6.4 g 二氧化硫气体所含的氧原子数为0.2 NA | |
| D. | 常温常压下,11.2 L 氯气含有的分子数为0.5 NA |
20.下列物品用到硅单质的是( )
| A. | 手机芯片 | B. | 光导纤维 | C. | 陶瓷餐具 | D. | 石英钟表 |
10.下列行为符合安全要求的是( )
| A. | 金属钠着火时,立即用沾水的毛巾覆盖 | |
| B. | 配制稀硫酸时将水倒入浓硫酸中并不断搅拌 | |
| C. | 不慎洒出的酒精在桌上着火时,立即用水扑灭 | |
| D. | 大量氯气泄漏时,迅速离开现场并尽量往高处去 |
17.在“空气质量日报”中,不被列入首要污染物的是( )
| A. | 二氧化硫 | B. | 氮氧化物 | C. | 可吸入颗粒物 | D. | 二氧化碳 |
7.下列各组物质中,不能满足组内任意两种物质间在一定条件下均能发生化学反应的是( )
物质 组别 | 甲 | 乙 | 丙 |
| A | Al(OH)3 | HCl | NaOH |
| B | NH3 | O2 | H2SO3 |
| C | SiO2 | NaOH | HCl |
| D | SO2 | Ca(OH)2 | NaHCO3 |
| A. | A | B. | B | C. | C | D. | D |
8.2011年3月11日日本发生了9.0级强地震.福岛第一核电站1号机组12日下午发生的氢气爆炸.随后在爆炸核电站周围检测到的放射性物质有碘131和铯137.碘131一旦被人体吸入,可能会引发甲状腺疾病.日本政府计划向核电站附近居民发放防止碘131辐射的药物碘片.
(1)Cs(铯)的最外层电子排布式为6s1,与铯同主族的前四周期(包括第四周期)的三种元素A、B、C的电离能如下表:
那么三种元素A、B、C的元素符号分别为Li、Na、K,形成其单质晶体的化学键类型是金属键.
(2)F与I同主族,BeF2与H2O都是由三个原子构成的共价化合物分子,二者分子中的中心原子Be和O的杂化方式分别是sp、sp3.
(3)与碘同主族的氯具有较高的活泼性,能够形成大量的含氯化合物,如金属氯化物,非金属氯化物等.BCl3是一种非金属氯化物,该物质分子中B-Cl键的键角为120°.
(4)碘131是碘单质,其晶胞结构如下图所示,该晶胞中含有4个I2分子;KI的晶胞结构如下图乙所示,每个K+紧邻6个I-.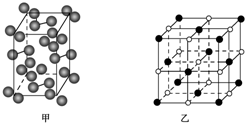
(1)Cs(铯)的最外层电子排布式为6s1,与铯同主族的前四周期(包括第四周期)的三种元素A、B、C的电离能如下表:
| 元素代号 | A | B | C |
| 第一电离能(kJ•mol-1) | 520 | 496 | 419 |
(2)F与I同主族,BeF2与H2O都是由三个原子构成的共价化合物分子,二者分子中的中心原子Be和O的杂化方式分别是sp、sp3.
(3)与碘同主族的氯具有较高的活泼性,能够形成大量的含氯化合物,如金属氯化物,非金属氯化物等.BCl3是一种非金属氯化物,该物质分子中B-Cl键的键角为120°.
(4)碘131是碘单质,其晶胞结构如下图所示,该晶胞中含有4个I2分子;KI的晶胞结构如下图乙所示,每个K+紧邻6个I-.

 .
.