题目内容
13.下列说法正确的是(NA 代表阿伏加德罗常数的值)( )| A. | 17g 氨气含有的原子总数为NA | |
| B. | 2.4 g 金属镁与氧气完全反应时失去电子总数为NA | |
| C. | 常温常压下,6.4 g 二氧化硫气体所含的氧原子数为0.2 NA | |
| D. | 常温常压下,11.2 L 氯气含有的分子数为0.5 NA |
分析 A.氨气分子含有4个原子,1mol氨气含有4mol原子;
B.镁为2价金属,1mol镁变成镁离子失去2mol电子;
C.根据n=$\frac{m}{M}$计算出二氧化硫的物质的量,再根据二氧化硫的分子组成计算出含有的氧原子数目;
D.常温常压下,不能使用标况下的气体摩尔体积计算氯气的物质的量.
解答 解:A.17g氨气的物质的量为1mol,含有4mol原子,含有的原子总数为4NA,故A错误;
B.2.4g镁的物质的量为0.1mol,0.1mol镁变成镁离子失去0.2mol电子,失去的电子数为0.2NA,故B错误;
C.6.4g二氧化硫的物质的量为0.1mol,含有0.2mol氧原子,所含的氧原子数为0.2NA,故C正确;
D.不是标准状况下,题中条件无法计算11.2L二氧化硫的物质的量,故D错误;
故选C.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下的气体摩尔体积的使用条件,阿伏加德罗常数是高考的“热点”,它既考查了学生对物质的量、粒子数、质量、体积等与阿伏加德罗常数关系的理解,又可以涵盖多角度的化学知识内容.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
3.在学习了物质及其变化之后,某学习小组认为化学反应反应中的先后顺序很重要.他们归纳了下面一些情况,你认为正确的是( )
| A. | 向浓度为0.1 mol/L 的FeI2溶液中通入Cl2,Fe2+先反应 | |
| B. | 向NH4Al(SO4)2溶液中滴加少量的NaOH溶液,NH4+先反应 | |
| C. | 向浓度均为0.1 mol/L的Na2CO3和NaOH混合溶液通入CO2气体,NaOH先反应 | |
| D. | 向等浓度的FeCl3溶液加入质量相等且颗粒大小相同的铁和铜,铜先反应 |
4.2014年10月8日,诺贝尔化学奖授予了三位超高分辨率荧光显微镜的贡献者,这是迄今人类玻璃显微镜的最高成就,玻璃属于( )
| A. | 纯净物 | B. | 混合物 | C. | 单质 | D. | 化合物 |
1.设NA代表阿伏加德罗常数,下列叙述正确的是( )
| A. | 0.1mol铁在氯气中完全反应失去的电子数为0.2NA | |
| B. | 常温常压下,1L 0.1mol•L-1氯化铝溶液中含有0.3 NA个Cl- | |
| C. | 标准状况下,22.4L氨水中含有NA个NH3分子 | |
| D. | 常温常压下,24g镁条投入足量稀硫酸中生成22.4L H2 |
8.下列离子方程式书写正确的是( )
| A. | 硫酸镁溶液跟氢氧化钡溶液反应:SO42-+Ba2+═BaSO4↓ | |
| B. | NaHCO3溶液与NaOH溶液反应:OH-+HCO3-═CO32-+H2O | |
| C. | AlCl3溶液中加入足量的氨水:Al3++4OH-═AlO2-+2H2O | |
| D. | FeCl2溶液跟Cl2反应:2Fe2++Cl2═2Fe3++2Cl- |
5.常温下,下列试剂的保存方法不正确的是( )
| A. | 氢氟酸保存于棕色玻璃瓶中 | B. | 新制的氯水保存于棕色玻璃瓶中 | ||
| C. | 实验室少量的钠保存于煤油中 | D. | 浓硝酸运输时保存在铝制容器中 |
2. 按如图所示实验装置进行钠跟水反应的实验,据此判断下列说法正确的是( )
按如图所示实验装置进行钠跟水反应的实验,据此判断下列说法正确的是( )
 按如图所示实验装置进行钠跟水反应的实验,据此判断下列说法正确的是( )
按如图所示实验装置进行钠跟水反应的实验,据此判断下列说法正确的是( )| A. | 打开右端胶塞,将一小块金属钠加入到煤油中,反应前片刻,钠的位置应在a处 | |
| B. | 开始反应后,能观察到的实验现象是钠在b处液面以下的水中反应 | |
| C. | 反应一段时间后,左端液面上升,进入长颈漏斗,a处有无色气体产生 | |
| D. | 若用苯或酒精来代替煤油,可观察到相同的实验现象 |
16.下列实验操作正确且能达到实验目的是( )
| 实验目的 | 操作 | |
| A | 比较水和乙醇中羟基氢的活泼性强弱 | 用金属钠分别与水和乙醇反应 |
| B | 欲证明CH2=CHCHO中含有碳碳双键 | 滴入KMnO4酸性溶液,看紫红色是否褪去 |
| C | 确定溴乙烷中含有溴元素 | 与NaOH溶液共热,再往混合液中滴加AgNO3溶液,观察是否有浅黄色沉淀生成 |
| D | 欲除去苯中混有的苯酚 | 向混合液中加入浓溴水,充分反应后,过滤 |
| A. | A | B. | B | C. | C | D. | D |
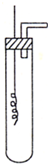 某学习小组为证明并观察铜与稀HNO3反应的产物是NO,设计了如图所示的
某学习小组为证明并观察铜与稀HNO3反应的产物是NO,设计了如图所示的