题目内容
8.如表实验现象所对应的离子方程式正确的是( )| 实验 | 现象 | 离子方程式 | |
| A | 稀硫酸滴入含酚酞的Ba(OH)2溶液中 | 白色沉淀生成,溶液由红色变无色 | Ba2++OH-+H++SO${\;}_{4}^{2-}$═BaSO4↓+H2O |
| B | 磁性氧化铁(Fe3O4)溶于氢碘酸 | 磁性氧化铁溶解,溶液变棕黄色 | Fe3O4+8H+═Fe2++2Fe3++4H2O |
| C | Ca(OH)2澄清溶液加到氯水中 | 溶液由黄绿色变为无色 | Cl2+2Ca(OH)2═Cl-+ClO-+Ca2++H2O |
| D | 稀硫酸加到KI淀粉溶液中 | 在空气中放置一段时间后,溶液呈蓝色 | 4H++4I-+O2═2I2+2H2O |
| A. | A | B. | B | C. | C | D. | D |
分析 A.不符合离子的配比;
B.发生氧化还原反应生成碘化亚铁、碘、水;
C.反应生成氯化钙、次氯酸钙、水,氢氧化钙完全电离;
D.发生氧化还原反应生成碘、水.
解答 解:A.稀硫酸滴入含酚酞的Ba(OH)2溶液中的离子反应为Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故A错误;
B.磁性氧化铁(Fe3O4)溶于氢碘酸的离子反应为2I-+Fe3O4+8H+═3Fe2++4H2O+I2,故B错误;
C.Ca(OH)2澄清溶液加到氯水中的离子反应为Cl2+2OH-═Cl-+ClO-+H2O,故C错误;
D.稀硫酸加到KI淀粉溶液中的离子反应为4H++4I-+O2═2I2+2H2O,故D正确;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.下列溶液加热蒸干后,不能析出溶质固体的是( )
| A. | Fe2(SO4)3 | B. | FeCl3 | C. | Na2CO3 | D. | KCl |
19.下列电离方程式书写正确的是( )
| A. | H2S?2H++S2- | B. | CH3COOH?H++CH3COO- | ||
| C. | NH3+H2O═NH${\;}_{4}^{+}$+OH- | D. | NaHCO3═Na++H++CO32- |
16.下列关于基本营养物质的说法中正确的是( )
| A. | 糖类、油脂、蛋白质都是高分子化合物 | |
| B. | 油脂是产生能量最高的营养物质,油脂水解得到高级脂肪酸和甘油 | |
| C. | 糖类、油脂、蛋白质都是只由C、H、O三种元素组成的 | |
| D. | 用米汤检验加碘食盐中的碘酸钾(KIO3) |
3.下列反应中,反应后固体物质增重的是( )
| A. | 二氧化碳通过Na2O2粉末 | B. | 铝与Fe2O3发生铝热反应 | ||
| C. | 碳与SiO2电炉中抽取粗硅 | D. | 将锌片投入CuSO4溶液中 |
20.在某100mL混合酸中,HN03物质的量浓度是4mol•L-1,H2SO4物质的量浓度是2mol•L-1,向其中加入19.2g铜粉微热,待充分反应后,则被还原的HNO3物质的量为( )
| A. | 0.4mol | B. | 0.2mol | C. | 0.225mol | D. | 无法计算 |
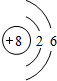 .
.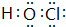 ,该化合物分子内存在共价键,E的钠盐属于离子化合物.
,该化合物分子内存在共价键,E的钠盐属于离子化合物.