题目内容
17.在标准状况下,1L丙烷和2L乙烷的混合气体在80L空气中完全燃烧,生成的气体经干燥后,其体积为( )| A. | 85L | B. | 75L | C. | 73L | D. | 70L |
分析 先写出燃烧的方程式,根据体质数据可知氧气过量,然后利用差量法分别计算出丙烷和乙烷完全燃烧后气体减少的总体积,然后计算出反应后的气体总体积即可.
解答 解:80L空气中约含有氧气的体积为:80L×$\frac{1}{5}$=16L,则氧气过量,
2C2H6+7O2$\stackrel{点燃}{→}$4CO2+6H2O△V
2 7 4 5
2L 10L
C3H8+5O2$\stackrel{点燃}{→}$3CO2+4H2O△V
1 5 3 3
1L 3L,
则1L丙烷和2L乙烷完全燃烧后气体总体积减少:10L+3L=13L,
所以反应后气体总体积为:80L+1L+2L-13L=70L,
故选D.
点评 本题考查了混合物反应的计算,题目难度中等,明确发生反应原理为解答关键,注意掌握差量法在化学计算中的应用方法,试题侧重考查学生的分析能力及化学计算能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.下列有关物质的性质、制取或应用等的说法中正确的是( )
| A. | 用10%的盐酸蒸发浓缩获得30%的盐酸 | |
| B. | 水晶项链和餐桌上的瓷盘都是硅酸盐制品 | |
| C. | 二氧化硫具有漂白性,与氯水混合使用效果更好 | |
| D. | 可利用丁达尔效应来区别淀粉溶液和氯化钠溶液 |
5.在溶液中能大量共存,若加入OH-就有沉淀析出,若加入H+就能放出气体的是( )
| A. | Mg2+、Na+、Cl-、CO32- | B. | Ba2+、K+、OH-、NO3- | ||
| C. | H+、Al3+、NH4+、SO42- | D. | Na+、Cl-、Ca2+、HCO3- |
12.下列排列顺序正确的是( )
| A. | 熔沸点:H2O>HF>HCl | B. | 原子半径:Mg>Na>O | ||
| C. | 酸性:H3PO4>H2SO4>HClO4 | D. | 热稳定性:H2O>HF>H2S |
4.乙酰苯胺可用作止痛剂、退热剂、防腐剂和染料中间体,实验室制备乙酰苯胺反应原理和有关数据如下: NH2+CHCOOH$\stackrel{△}{?}$
NH2+CHCOOH$\stackrel{△}{?}$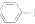
 +H2O
+H2O
实验步骤:
在50ml圆底烧瓶中加入无水苯胺5ml.,冰醋酸7.5mL,锌粉0.lg,按下图安装仪器,加入沸石,给反应器均匀加热,使反应液在微沸状态下回流,调节加热温度,使柱顶温度控制在105℃左右,反应约60~80nun,当反应基本完成时,停止加热.
在搅拌下,趁热将烧瓶中的物料倒人盛有l00mL冰水的烧杯中,剧烈搅拌,并冷却烧杯至室温,粗乙酰苯胺结晶析出,抽滤、洗涤、干燥,得到乙酰苯胺粗品.将粗品重结晶,抽滤,晾干,称重,计算产率,
注:D为刺形分馏柱,用于沸点差别不太大的混合物的分离. ,
,
请回答下列问题:
(1)仪器A的名称冷凝管,
(2)装置图中加热可用油浴(填“水浴”或“油浴”).
(3)实验中加入锌粉的目的是防止苯胺在反应过程中被氧化.
(4)为何要控制分馏柱上端的温度在105℃左右不断分出反应过程中生成的水,促进反应正向进行,提高生成物的产率.
(5)通过观察到温度计温度下降或锥形瓶内液体不再增加,现象可判断反应基本完成,反应结束后须立即倒入事先准备好的冰水中的原因乙酰苯胺的熔点较高,稍冷即会固化,凝固在烧瓶中难易倒出.
(6)洗涤乙酰苯胺粗品最合适的试剂是a.
a.用少量冷水洗 b.用少量热水洗c.先用冷水洗,再用热水洗 d.用酒精洗
(7)该实验最终得到纯品1.8g,则乙酰苯胺的产率是24%.
 NH2+CHCOOH$\stackrel{△}{?}$
NH2+CHCOOH$\stackrel{△}{?}$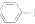
 +H2O
+H2O| 名称 | 相对分子质量 | 性状 | 密度/(g/cm3) | 熔点/℃ | 沸点/℃ | 溶解度 | |
| 苯胺 | 93 | 无色油状液体具有还原性 | 1.02 | -6.1 | 184 | 微溶于水 | 均易溶于乙醇、乙醚 |
| 乙酸 | 60 | 无色液体 | 1.05 | 16.5 | 118 | 易溶于水 | |
| 乙酰 苯胺 | 135 | 白色晶体 | 1.22 | 114 | 304 | 微溶于冷水,溶于热水 | |
在50ml圆底烧瓶中加入无水苯胺5ml.,冰醋酸7.5mL,锌粉0.lg,按下图安装仪器,加入沸石,给反应器均匀加热,使反应液在微沸状态下回流,调节加热温度,使柱顶温度控制在105℃左右,反应约60~80nun,当反应基本完成时,停止加热.
在搅拌下,趁热将烧瓶中的物料倒人盛有l00mL冰水的烧杯中,剧烈搅拌,并冷却烧杯至室温,粗乙酰苯胺结晶析出,抽滤、洗涤、干燥,得到乙酰苯胺粗品.将粗品重结晶,抽滤,晾干,称重,计算产率,
注:D为刺形分馏柱,用于沸点差别不太大的混合物的分离.
 ,
,请回答下列问题:
(1)仪器A的名称冷凝管,
(2)装置图中加热可用油浴(填“水浴”或“油浴”).
(3)实验中加入锌粉的目的是防止苯胺在反应过程中被氧化.
(4)为何要控制分馏柱上端的温度在105℃左右不断分出反应过程中生成的水,促进反应正向进行,提高生成物的产率.
(5)通过观察到温度计温度下降或锥形瓶内液体不再增加,现象可判断反应基本完成,反应结束后须立即倒入事先准备好的冰水中的原因乙酰苯胺的熔点较高,稍冷即会固化,凝固在烧瓶中难易倒出.
(6)洗涤乙酰苯胺粗品最合适的试剂是a.
a.用少量冷水洗 b.用少量热水洗c.先用冷水洗,再用热水洗 d.用酒精洗
(7)该实验最终得到纯品1.8g,则乙酰苯胺的产率是24%.
11.某工厂对制革工业污泥中Cr(Ⅲ)回收与再利用工艺流程如下(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Al3+、Mg2+):
已知:①+3价Cr在酸性溶液中性质稳定,当pH>9时以CrO42-形式存在且易氧化;
②常温下,部分阳离子以氢氧化物形式沉淀是溶液的pH如下:
(1)实验室用18.4mol•L-1的浓硫酸配制250mL 4.8mol•L-1的硫酸溶液,所用的玻璃仪器除烧杯、玻璃棒和吸量管(一种能精确量取一定体积液体的仪器)外,还需量筒、250mL容量瓶、胶头滴管;
(2)滤渣II是Fe(OH)3、Al(OH)3,过滤II步骤能否省略,为什么?
不能,当pH=8时,Al3+已经完全转化为沉淀,若不经过滤除去,当继续加入NaOH时,Al(OH)3会溶解,引入杂质离子AlO2-.
(3)写出滤液中加入H2O2发生反应的两种方程式2Cr3++3H2O2+H2O=Cr2O72-+8H;
(4)取得到的Na2CrO4晶体0.48g,加入硫酸溶液得到Na2CrO溶液,用0.3000 mol•L-1滴定至终点时(铬被还原为Cr3+),消耗20.00mL标准溶液.
①盛装FeSO4标准溶液应用酸式滴定管(填“酸式”或“碱式”),滴定时的操作为:左手控制活塞,右手震荡锥形瓶,眼睛注视锥形瓶内颜色变化,滴定至终点时,记录标准液的体积;
②计算该产品中Na2CrO4的质量分数为66.67%.

已知:①+3价Cr在酸性溶液中性质稳定,当pH>9时以CrO42-形式存在且易氧化;
②常温下,部分阳离子以氢氧化物形式沉淀是溶液的pH如下:
| 阳 | Fe | Mg | Al | Cr |
| 开始沉淀时的H | 1.9 | 9.0 | -- | -- |
| 沉淀完全时的H | 3. | 11.1 | 8 | 9 (>9溶解) |
(2)滤渣II是Fe(OH)3、Al(OH)3,过滤II步骤能否省略,为什么?
不能,当pH=8时,Al3+已经完全转化为沉淀,若不经过滤除去,当继续加入NaOH时,Al(OH)3会溶解,引入杂质离子AlO2-.
(3)写出滤液中加入H2O2发生反应的两种方程式2Cr3++3H2O2+H2O=Cr2O72-+8H;
(4)取得到的Na2CrO4晶体0.48g,加入硫酸溶液得到Na2CrO溶液,用0.3000 mol•L-1滴定至终点时(铬被还原为Cr3+),消耗20.00mL标准溶液.
①盛装FeSO4标准溶液应用酸式滴定管(填“酸式”或“碱式”),滴定时的操作为:左手控制活塞,右手震荡锥形瓶,眼睛注视锥形瓶内颜色变化,滴定至终点时,记录标准液的体积;
②计算该产品中Na2CrO4的质量分数为66.67%.

8. 粗铜中一般含有锌、铁、银、金等杂质.在如图所示的装置中,甲池的总反应方程式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O.接通电路一段时间后,纯Cu电极质量增加了3.2g.在此过程中,下列说法正确的是( )
粗铜中一般含有锌、铁、银、金等杂质.在如图所示的装置中,甲池的总反应方程式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O.接通电路一段时间后,纯Cu电极质量增加了3.2g.在此过程中,下列说法正确的是( )
 粗铜中一般含有锌、铁、银、金等杂质.在如图所示的装置中,甲池的总反应方程式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O.接通电路一段时间后,纯Cu电极质量增加了3.2g.在此过程中,下列说法正确的是( )
粗铜中一般含有锌、铁、银、金等杂质.在如图所示的装置中,甲池的总反应方程式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O.接通电路一段时间后,纯Cu电极质量增加了3.2g.在此过程中,下列说法正确的是( )| A. | 甲池中电解质溶液的pH值减小 | |
| B. | 乙池中CuSO4溶液的浓度不变 | |
| C. | 甲池中理论上消耗空气的体积是2.8L(空气中O2体积分数以20%计算) | |
| D. | 甲池通入CH3OH一极的电极反应为:CH3OH-6e-+2H2O═CO32-+8H+ |
9.关于下列各装置图的叙述中,正确的是( )
| A. | 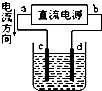 装置中,d为阳极、c为阴极 | |
| B. | 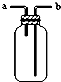 装置由a进气可用于收集H2、NH3、CO2、Cl2 等气体 | |
| C. | 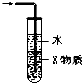 装置中X若为CCl4,可用于吸收NH3 或HCl,并可防止倒吸 | |
| D. | 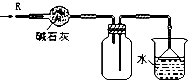 装置可用于干燥、收集HCl,并吸收多余的HCl |