题目内容
2.如图是四种常见有机物的比例模型示意图.下列说法正确的是( )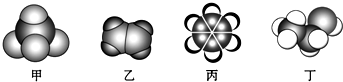
| A. | 甲能使酸性高锰酸钾溶液褪色 | |
| B. | 乙可与酸性高锰酸钾发生加成反应 | |
| C. | 丙中的碳碳键是介于碳碳单键和碳碳双键之间的独特的键 | |
| D. | 丁可与乙酸发生中和反应 |
分析 根据模型知,甲是甲烷或四氯化碳、乙是乙烯、丙是苯、丁是乙醇,
A.甲烷或四氯化碳都不含不饱和键,和酸性高锰酸钾不反应;
B.碳碳双键能被酸性高锰酸钾溶液氧化;
C.苯中碳碳键是特殊的化学键;
D.丁是乙醇,能和乙酸发生酯化反应.
解答 解:根据模型知,甲是甲烷或四氯化碳、乙是乙烯、丙是苯、丁是乙醇,
A.甲烷或四氯化碳都不含不饱和键,性质较稳定,和酸性高锰酸钾不反应,故A错误;
B.乙是乙烯,含有碳碳双键,性质较活泼,碳碳双键能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,故B错误;
C.苯中碳碳键是介于单键和双键之间的特殊化学键,导致能发生取代反应和加成反应,故C正确;
D.丁是乙醇,能和乙酸发生酯化反应或取代反应,和乙酸不发生中和反应,故D错误;
故选C.
点评 本题考查有机物结构和性质,明确官能团及其性质关系是解本题关键,熟悉常见有机物结构及其性质,题目难度不大.

练习册系列答案
相关题目
12.关于下列各图的叙述正确的是( )
| A. | 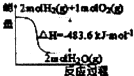 表示H2与O2发生反应过程中的能量变化,则H2的标准燃烧热为△H=-483.6kJ•mol-1 | |
| B. | 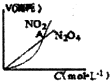 表示恒温恒容条件下发生的可逆反应2NO2?N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 | |
| C. | 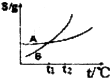 表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数B>A | |
| D. | 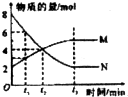 图中在t2时刻正反应速率大于逆反应速率 |
13.据报道,在40GPa高压下,用激光器加热到1800K,科学家已成功合成出CO2原子晶体,下列有关这种CO2晶体推断正确的是( )
| A. | 易液化,可用作制冷材料 | |
| B. | CO2晶体中,每个C原子周围结合2个O原子,每个O原子跟1个C原子结合 | |
| C. | 硬度很大,可用作耐磨材料 | |
| D. | 在一定条件下,CO2分子晶体转化为原子晶体是物理变化 |
10.有机物CH2=CH-CH2-CH(OH)-COOH可发生下列反应中的哪几类( )
(1)使溴水褪色 (2)使高锰酸钾溶液褪色 (3)与钠反应 (4)加聚反应
(5)酯化反应 (6)水解反应 (7)取代反应.
(1)使溴水褪色 (2)使高锰酸钾溶液褪色 (3)与钠反应 (4)加聚反应
(5)酯化反应 (6)水解反应 (7)取代反应.
| A. | 除(7)外都可以 | B. | 除(6)外都可以 | C. | (1)(2)(3)(7) | D. | (1)(2)(3)(5) |
17.下列说法正确的是( )
| A. | 原子最外层电子数为2的元素一定处于周期表ⅡA族 | |
| B. | 同周期第IA族元素与第ⅦA族元素形成的是离子化合物 | |
| C. | 硫化氢的沸点比水的沸点高 | |
| D. | 同主族元素形成的氧化物的晶体类型均相同 |
7.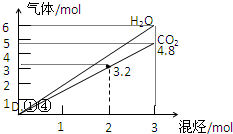 两种气态烃组成的混合气体完全燃烧后得到CO2和H2O的物质的量随混合烃的总物质的量的变化如图所示,
两种气态烃组成的混合气体完全燃烧后得到CO2和H2O的物质的量随混合烃的总物质的量的变化如图所示,
则下列对混合烃的判断正确的是( )
①一定有乙烯;②一定有甲烷;③一定有丙烷;
④一定无乙烷;⑤可能有乙烷;⑥可能有丙炔.
 两种气态烃组成的混合气体完全燃烧后得到CO2和H2O的物质的量随混合烃的总物质的量的变化如图所示,
两种气态烃组成的混合气体完全燃烧后得到CO2和H2O的物质的量随混合烃的总物质的量的变化如图所示,则下列对混合烃的判断正确的是( )
①一定有乙烯;②一定有甲烷;③一定有丙烷;
④一定无乙烷;⑤可能有乙烷;⑥可能有丙炔.
| A. | ②③⑤ | B. | ⑤⑥ | C. | ②④⑥ | D. | ①④ |
14.等质量的下列烃完全燃烧时,消耗氧气的量最多的是( )
| A. | CH4 | B. | C2H4 | C. | C3H4 | D. | C6H6 |
11.下列反应或过程对能量的变化如图所示的是( )


| A. | H+H→H-H | B. | 2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2H2O | ||
| C. | Mg+2HCl=MgCl2+H2↑ | D. | H2SO4+2KOH=K2SO4+2H2O |
13.“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池.如图为RFC工作原理示意图,有关说法正确的是( )
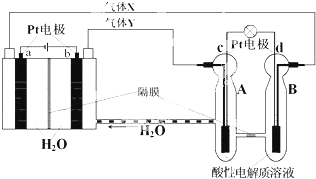

| A. | 转移0.1mol电子时,a电极产生1.12LH2 | |
| B. | b电极上发生的电极反应是:2H2O+2e-=H2↑+2OH- | |
| C. | c电极上进行还原反应,B电池中的H+可以通过隔膜进入A池 | |
| D. | d电极上发生的电极反应是:O2+4H++4e-=2H2O |