题目内容
【题目】偏二甲肼与![]() 是常用的火箭推进剂,二者发生如下化学反应:
是常用的火箭推进剂,二者发生如下化学反应:
![]()
![]()
(1)火箭残骸中常现红棕色气体,原因为:![]()
![]()
当温度升高时,气体颜色变深,则反应![]() 为____
为____![]() 填“吸热”或“放热”
填“吸热”或“放热”![]() 反应。
反应。
(2)在一个体积为1L的恒压密闭容器中充入![]() ,一段时间后达化学平衡状态,反应的化学平衡常数表达式
,一段时间后达化学平衡状态,反应的化学平衡常数表达式![]() _________;反应3s后
_________;反应3s后![]() 的物质的量为
的物质的量为![]() ,则
,则![]() 内的平均反应速率
内的平均反应速率![]() ______
______
(3)在![]() 的平衡体系中,回答下列问题:
的平衡体系中,回答下列问题: ![]() 填“正向”、“逆向”、“不”
填“正向”、“逆向”、“不”![]()
①在溶液中加入少量的KSCN固体,平衡____移动。
②在溶液中加入少量的NaOH固体,平衡_____移动。
【答案】吸热 ![]() 0.1mol/L
0.1mol/L![]() s 正向 逆向
s 正向 逆向
【解析】
(1)对于反应![]()
![]() ,当温度升高时,气体颜色变深,说明平衡向正向移动,根据勒夏特列原理,升温向吸热方向移动,故正反应吸热;
,当温度升高时,气体颜色变深,说明平衡向正向移动,根据勒夏特列原理,升温向吸热方向移动,故正反应吸热;
(2)反应![]()
![]() 的平衡常数表达式为
的平衡常数表达式为![]() ;反应3s后
;反应3s后![]() 的物质的量为
的物质的量为![]() ,则N2O4的物质的量变化为0.3mol,浓度变化Δc=
,则N2O4的物质的量变化为0.3mol,浓度变化Δc=![]() ,反应速率
,反应速率![]() ;
;
(3)①加入少量的KSCN固体,溶液中SCN-的浓度增大,根据勒夏特列原理,平衡正向移动;
②加入少量的NaOH固体,OH-与Fe3+沉淀,使Fe3+浓度减小,根据勒夏特列原理,平衡逆向移动;

 阅读快车系列答案
阅读快车系列答案【题目】(1)已知反应:Na2S2O3+H2SO4=Na2SO4+S↓+SO2+H2O。甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响。设计实验如下:
实验编号 | 实验温度/℃ | c(Na2S2O3)/mol·L-1 | V(Na2S2O3)/mL | c(H2SO4)/mol·L-1 | V(H2SO4)/mL | V(H2O)/mL |
① | 25 | 0.1 | 5.0 | 0.1 | 10.0 | a |
② | 25 | 0.1 | 10.0 | 0.1 | 10.0 | 0 |
③ | 25 | 0.2 | 5.0 | 0.1 | 5.0 | b |
④ | 50 | 0.2 | 5.0 | 0.1 | 10.0 | 5.0 |
其他条件不变时:探究温度对化学反应速率的影响,应选择实验__________(填实验编号);若同时选择实验①②、实验②③,测定混合液变浑浊的时间,可分别探究Na2S2O3浓度和H2SO4的浓度对化学反应速率的影响,则表中a和b分别为________和________。
(2)某同学设计如下实验流程探究Na2S2O3的化学性质。
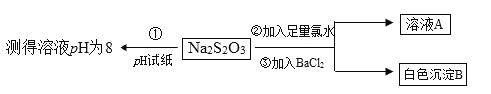
实验操作①中测试时pH试纸的颜色应该接近_____________。
A.红色 B.黄色 C.深蓝色 D.绿色
上述流程中实验②、③的目的是为了探究Na2S2O3某种化学性质,你认为是探究了Na2S2O3的_____性。