题目内容
【题目】工业尾气SO2有多种吸收和处理方法。

(1)亚硫酸钠吸收法
写出Na2SO3溶液吸收SO2的离子方程式:________________。
(2)电化学处理法
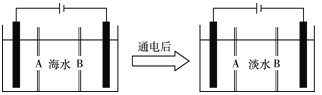
①如图所示,Pt(1)电极的反应式为:____________________。
②当电路中转移0.02 mol e-时(较浓H2SO4尚未排出),交换膜左侧溶液中约增加________mol离子。
(3)在甲酸钠、氢氧化钠混合溶液中通入二氧化硫气体可以制备工业产品保险粉(Na2S2O4),同时生成二氧化碳气体,写出该反应的离子方程式:______________________。
【答案】
(1)SO32-+SO2+H2O===2HSO3-
(2)①SO2-2e-+2H2O===4H++SO42-;②0.03 mol
(3)HCOO-+2SO2+OH-===S2O42-+CO2+H2O
【解析】
试题分析:(1)Na2SO3溶液吸收SO2的离子方程式为SO32-+SO2+H2O=2HSO3-,故答案为:SO32-+SO2+H2O=2HSO3-;
(2)①由图可知,Pt(1)电极上二氧化硫被氧化生成硫酸,电极反应式为:SO2 - 2e- + 2H2O = SO42- + 4 H+,故答案为:SO2 - 2e- + 2H2O = SO42- + 4H+;
②左侧电极反应式为:SO2-2e-+2H2O=SO42-+4H+,根据电子转移守恒,生成硫酸根物质的量![]() =0.01mol,生成氢离子为0.04mol,为保持溶液电中性,0.01mol硫酸根需要0.02mol氢离子,多余的氢离子通过阳离子交换膜移至右侧,即有0.02mol氢离子移至右侧,故左侧溶液中增加离子为0.01mol+0.02mol=0.03mol,故答案为:0.03;
=0.01mol,生成氢离子为0.04mol,为保持溶液电中性,0.01mol硫酸根需要0.02mol氢离子,多余的氢离子通过阳离子交换膜移至右侧,即有0.02mol氢离子移至右侧,故左侧溶液中增加离子为0.01mol+0.02mol=0.03mol,故答案为:0.03;
(3)甲酸钠和氢氧化钠混合溶液与SO2生成保险粉Na2S2O4同时生成二氧化碳,反应的离子方程式:HCOO-+OH-+2SO2═S2O42-+H2O+CO2故答案为:HCOO-+OH-+2SO2═S2O42-+H2O+CO2。

 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案【题目】常温下,下列各组物质中,Y既能与X反应又能与Z反应的是( )
X | Y | Z | |
① | NaOH溶液 | Al(OH)3 | 稀硫酸 |
② | KOH溶液 | SiO2 | 浓盐酸 |
③ | O2 | N2 | H2 |
④ | FeCl3溶液 | Cu | 浓硝酸 |
A. ①③ B. ①④ C. ②④ D. ②③