题目内容
【题目】南海某小岛上,解放军战士为了寻找合适的饮用水源,对岛上山泉水进行分析化验,结果显示水的硬度为28°(属于硬水),主要含钙离子、镁离子、氯离子和硫酸根离子。请思考下列问题:
(1)该泉水属于________硬水(填写“暂时”或“永久”)。
(2)若要除去Ca2+、Mg2+可以往水中加入石灰和纯碱,试剂添加时先加________后加________,原因是______________________。
(3)目前常用阳离子交换树脂如NaR、HR来进行水的软化,若使用HR作为阳离子交换树脂,则水中的Ca2+、Mg2+与交换树脂的________起离子交换作用。若使用NaR作为阳离子交换树脂,失效后可放入5%~8%________溶液中再生。
(4)岛上还可以用海水淡化来获得淡水。下面是海水利用电渗析法获得淡水的原理图,已知海水中含Na+、Cl-、Ca2+、Mg2+、SO等离子,电极为惰性电极。请分析下列问题:
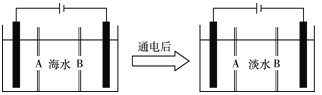
① 阳离子交换膜是指________(填A或B)。
②写出通电后阳极区的电极反应式:__________;阴极区的现象是:____________。
【答案】(1)永久 (2)石灰 纯碱 过量的钙离子可通过纯碱沉淀下来 (3)H+ NaCl (4)①B
②2Cl--2e- =Cl2↑ 电极上产生无色气体,溶液中出现少量白色沉淀
【解析】
试题分析:(1)由较多钙离子和镁离子以及硫酸根离子引起的硬水,属于永久硬水。
(2)纯碱除了除去原溶液中的Ca2+还要除去加入的Ca2+,因此一定把纯碱放在石灰的后面加入。
(3)利用阳离子交换原理,将失效后的NaR放入NaCl的溶液中,使其获得再生。
(4)①通电后,阳离子Na+向着阴极移动,故B为阳离子交换膜;
②电解时,阴离子Cl-在阳极失电子生成Cl2,电极反应式为2Cl--2e- =Cl2↑;阴极区H+得电子,生成H2同时产生OH-,与Mg2+和Ca2+反应生成氢氧化镁和氢氧化钙沉淀。

【题目】下表所列各组物质中,物质之间通过一步反应能实现如图所示转化的是 ( )

X | Y | Z | |
① | Cu | CuO | Cu(OH)2 |
② | CH3CH2OH | CH3CHO | CH2=CH2 |
③ | Na2CO3 | NaOH | NaHCO3 |
④ | CaCO3 | CaO | Ca(OH)2 |
A.②③ B.③④ C.②④ D.①②



