题目内容
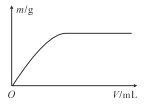
【题目】已知HA的酸性强于HB的酸性。25℃时,用NaOH固体分别改变物质的量浓度均为0.1molL-l的HA溶液和HB溶液的pH(溶液的体积变化忽略不计),溶液中A-、B-的物质的量浓度的负对数与溶液的pH的变化情况如图所示。下列说法正确的是

A.曲线I表示溶液的pH与-lgc(B-)的变化关系
B.![]()
C.溶液中水的电离程度:M>N
D.N点对应的溶液中c(Na+)>Q点对应的溶液中c(Na+)
【答案】B
【解析】
A.HA的酸性强于HB的酸性,则Ka(HA)>Ka(HB),当-1gc(A-)=-1gc(B-)时c(A-)=c(B-),c(HA)=c(HB),则c(H+)越大,pH越小,Ka越大,所以曲线II表示pH与-1gc(B-)的关系,故A错误;
B.对于HB,取点(10,2),则c(H+)=10-10mol/L,c(B-)=10-2mol/L,则Ka(HB)=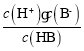 =
=![]() ,同理对于HA,取点(8,2),则c(H+)=10-8mol/L,c(A-)=10-2mol/L,则Ka(HA)=
,同理对于HA,取点(8,2),则c(H+)=10-8mol/L,c(A-)=10-2mol/L,则Ka(HA)=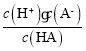 =
=![]() ,所以Ka(HA):Ka(HB)=100,故B正确;
,所以Ka(HA):Ka(HB)=100,故B正确;
C.M点和N点溶液中c(A-)=c(B-),溶液pH越大,水的电离程度越大,所以水的电离程度M<N,故C错误;
D.对于N点溶液,存在电荷守恒:c(Na+)+c(H+)=c(OH-)+c(B-),对于Q点溶液,存在电荷守恒:c(Na+)+c(H+)=c(OH-)+c(A-),N点和Q点溶液pH相同,则两溶液中c(H+)和c(OH-)分别相等,但c(B-)<c(A-),则N点对应的溶液中c(Na+)<Q点对应的溶液中c(Na+),故D错误;
故选:B。

【题目】H2S是石油化工行业广泛存在的污染性气体,但同时也是重要的氢源和硫源,工业上可以采取多种方式处理。
Ⅰ.干法脱硫
(1)已知H2S的燃烧热为akJmol-1 ,S的燃烧热为bkJmol-1 ,则常温下空气直接氧化脱除H2S的反应:2H2S(g)+O2(g)=2S(s)+2H2O(l) △H=______kJmol-1 。
(2)常用脱硫剂的脱硫效果及反应条件如下表,最佳脱硫剂为_________。
脱硫剂 | 出口硫(mg·m-3) | 脱硫温度(℃) | 操作压力(MPa) | 再生条件 |
一氧化碳 | <1.33 | 300~400 | 0~3.0 | 蒸气再生 |
活性炭 | <1.33 | 常温 | 0~3.0 | 蒸气再生 |
氧化锌 | <1.33 | 350~400 | 0~5.0 | 不再生 |
锰矿 | <3.99 | 400 | 0~2.0 | 不再生 |
Ⅱ.热分解法脱硫
在密闭容器中,充入一定量的H2S气体,发生热分解反应H2S(g)![]() 控制不同的温度和压强进行实验,结果如图(a)。
控制不同的温度和压强进行实验,结果如图(a)。
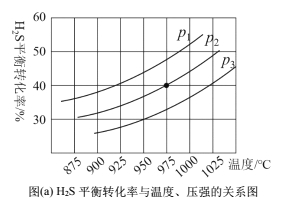
(3)图(a)中压强关系p1、p2、p3由大到小的顺序为______,该反应为____(填“吸热”或“放热”)反应,若要进一步提高H2S的平衡转化率,除了改变温度和压强外,还可以采取的措施有_______。
(4)压强为p、温度为975℃时,![]() 的平衡常数K=0.04,则起始浓度c=______molLˉ1,若向容器中再加入1molH2S气体,相同温度下再次达到平衡时,K_____0.04(填“>”1 “<”或“=”)。
的平衡常数K=0.04,则起始浓度c=______molLˉ1,若向容器中再加入1molH2S气体,相同温度下再次达到平衡时,K_____0.04(填“>”1 “<”或“=”)。
Ⅲ.间接电解法脱硫
间接电解法是通过FeCl3溶液吸收并氧化H2S气体,将反应后溶液通过电解再生,实现循环使用,该法处理过程如下图(b)。
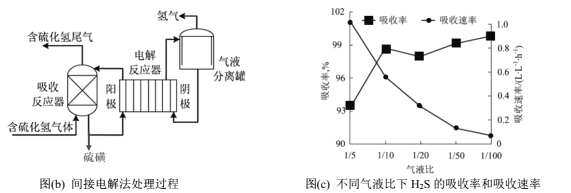
(5)电解反应器总反应的离子方程式为________。
(6)气液比为气体与液体的流速比,吸收反应器内液体流速固定。测定吸收器中相同时间内不同气液比下H2S的吸收率和吸收速率,结果如图(c)所示,随着气液比减小,H2S的吸收速率逐渐降低,而吸收率呈上升趋势的原因为____________。