题目内容
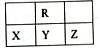
几种短周期元素的原子半径及主要化合价如下表:
下列叙述正确的是
A.W的气态氢化物比Z的气态氢化物稳定
B.X、Y元素的金属性X<Y
C.Y的最高价氧化物对应的水化物能溶于稀氨水
D.一定条件下,Z单质与W的常见单质直接生成ZW2
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
| 元素化合物的性质 |  | 形成常见的两性氧化物 | Z2是常见保护气 | W3可用于杀菌消毒 |
下列叙述正确的是
A.W的气态氢化物比Z的气态氢化物稳定
B.X、Y元素的金属性X<Y
C.Y的最高价氧化物对应的水化物能溶于稀氨水
D.一定条件下,Z单质与W的常见单质直接生成ZW2
A
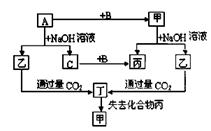
试题分析:O3具有强氧化性,可用于杀菌消毒,则W是氧,N2是常见保护气,则Z是氮,第二周期元素中,氧元素的非金属性比氮强,则氧元素的气态氢化物比氮元素的气态氢化物稳定,故A正确;Al2O3是常见的两性氧化物,则Y是铝,根据最高正价等于主族序数,根据原子半径推断X是镁,第三周期元素中镁的金属性大于铝,故B错误;稀氨水是弱碱溶液,氢氧化铝是两性氢氧化物,后者能溶于盐酸、氢氧化钠等强酸、强碱溶液,不溶于弱碱溶液和弱酸溶液,故C错误;氮气与氧气在放电或高温下反应,直接生成一氧化氮,不能直接变为二氧化氮,故D错误。

练习册系列答案
相关题目