题目内容
下列有关反应热的说法正确的是( )
| A.任何强酸与强碱反应生成1 mol H2O的过程中,放出的热量均相同 |
| B.等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| C.对于任何一个吸热反应,使用催化剂后,ΔH将降低 |
| D.已知:O=O键键能为a kJ/ mol、H-H键键能为b kJ/ mol、水蒸气中H-O键能为c kJ/ mol。又知:H2O(g)= H2O(l)ΔH=" -d" kJ/ mol。则反应2H2 (g) + O2(g) = 2H2O(l) 的ΔH为:(a+2b-4c-2d)kJ/ mol |
D
解析试题分析:A、只有稀强酸与稀强碱反应生成1mol水的过程中,放出的热量相同,错误;B、相同条件下, 同一物质在气态时的能量最多、液态次之、固态最少,反应放出的热量等于反应物的能量减去生成物 的能量,因为生成物相同,所以等量的硫蒸汽和硫固体分别完全燃烧,前者放出的热量多,错误;C、 催化剂的作用是加快反应速率,与反应的热效应无关,错误;D、正确。
考点:反应热。

练习册系列答案
相关题目
氢化热是指一定条件下,1 mol 不饱和化合物加氢时放出的热量。表中是环己烯( )、环己二烯(
)、环己二烯( )和苯的氢化热数据。
)和苯的氢化热数据。
| 化合物 | 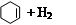  | 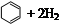  | 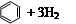  |
| 氢化热 (kJ/mol) | 119.7 | 232.7 | 208.4 |
根据表中数据推断正确的是
A.环己二烯与H2的反应最剧烈
B.环己烯、环己二烯和苯有相同的官能团
C.三种化合物中环己二烯的稳定性最强
D.上述条件下,1 mol
 转变为
转变为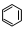 时放热
时放热 如下图所示,△H1=-393.5 kJ?mol-1,△H2=-395.4 kJ?mol-1,下列说法或表示式正确的是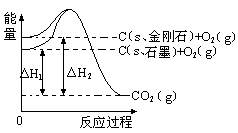
| A.石墨和金刚石的转化是物理变化 |
| B.1mol石墨的总能量比1 mol金刚石的总能量大1.9 kJ |
| C.金刚石的稳定性强于石墨 |
| D.C(s、石墨)=C(s、金刚石) △H=" +1.9" kJ?mol-1 |
相同温度下,甲(恒容)、乙(恒压)、丙(恒容)3个密闭容器中发生可逆反应:
2SO2(g)+O2(g) 2SO3(g)ΔH =" -197" kJ/mol。实验测得起始、平衡时的有关数
2SO3(g)ΔH =" -197" kJ/mol。实验测得起始、平衡时的有关数
据如下表。下列正确的是
| 容器 | 起始各物质的物质的量/mol | 达到平衡时体系能量的变化 | ||
| SO2 | O2 | Ar | ||
| 甲 | 2 | 1 | 0 | 放出热量:Q1 |
| 乙 | 2 | 1 | 0 | 放出热量:Q2 |
| 丙 | 2 | 1 | 0.5 | 放出热量:Q3 |
A.Q1 =Q3<Q2
B.达到平衡时,乙容器中SO2的体积分数最大
C.平衡时,甲、乙、丙3个容器中甲的平衡常数最小
D.若在上述条件下,反应生成1molSO3(s),则反应放热为98.5kJ
下列各表述与示意图一致的是
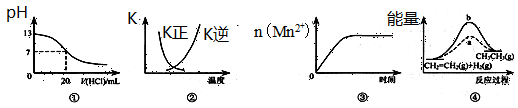
| A.图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,溶液的pH随加入酸体积的变化 |
B.图②中曲线表示反应2SO2(g) + O2(g)  2SO3(g);ΔH<0 正、逆反应的平衡常数K随温度的变化 2SO3(g);ΔH<0 正、逆反应的平衡常数K随温度的变化 |
| C.图③表示10 mL 0.01 mol·L-1 KMnO4酸性溶液与过量的0.1 mol·L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化 |
| D.图④中a、b曲线分别表示反应CH2=CH2 (g) + H2(g)→CH3CH3(g);ΔH<0使用和未使用催化剂时,反应过程中的能量变化 |
25℃、101kPa下,2g氢气燃烧生成液态水,放出285.8 kJ热量,表示该反应的热化学方程式正确的是
| A.2H2(g)+O2(g)=2H2O(l)△H=-285.8 kJ/mol |
| B.2H2(g)+O2(g)=2H2O(l)△H=+571.6 kJ/mol |
| C.2H2(g)+O2(g)=2H2O(g)△H=-571.6kJ/mol |
D.H2(g)+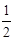 O2(g)=H2O(l)△H=-285.8 kJ/mol O2(g)=H2O(l)△H=-285.8 kJ/mol |
一定条件下,充分燃烧一定量的丁烷放出QkJ的热量,经测定完全吸收生成的二氧化碳需消耗5 mol·L-1的KOH溶液100 mL,恰好生成正盐。则此条件下反应C4H10(g)+13/2O2(g) = 4CO2(g)+5H2O(g)的ΔH为( )
| A.+8Q kJ·mol-1 | B.+16Q kJ·mol-1 | C.-8Q kJ·mol-1 | D.-16Q kJ·mol-1 |
下列依据热化学方程式得出的结论正确的是( )
| A.已知2H2(g)+O2(g)=2H2O(g);△H=-483.6 kJ·mol-1,则氢气的燃烧热为241.8 kJ·mol-1 |
| B.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l);△H=-57.3 kJ·mol-1 则含40.0g NaOH的稀溶液与稀醋酸完全中和,放出57.3kJ的热量 |
| C.已知C(石墨,s)=C(金刚石,s);△H>0,则石墨比金刚石稳定 |
| D.己知2C(s)+2O2(g)=2CO2(g));△H=a、2C(s)+O2(g)=2CO(g);△H=b,则a>b |
下列依据热化学方程式得出的结论正确的是( )
A.已知2SO2(g)+O2 2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量 2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量 |
| B.已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定 |
| C.已知H+(aq)+OH-(aq)=H2O(1)△H=-57.3kJ/mol,则任何酸碱中和的反应热均为57.3kJ |
| D.已知2C(s)+2O2(g)=2CO2(g)△H1 |