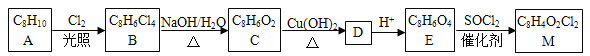题目内容
【题目】为探究某固体X(仅含两种短周期元素)的组成和性质。设计并完成如下实验:
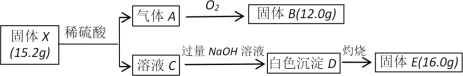
已知:气体A为氢化物,固体B是光导纤维的主要成分,固体E为耐高温材料。
请回答:
(1)固体X的化学式为__________。
(2)写出反应C→D的离子方程式__________。
(3)已知NH3与气体A在一定条件下反应后可得到一种耐高温材料(仅含两种元素,摩尔质量为140 g·mol-1)和H2,写出该反应的化学方程式__________。
【答案】Mg2Si Mg2+ + 2OH- = Mg(OH)2↓ 3SiH4+4NH3= Si3N4+12H2↑
【解析】
固体B是光导纤维的主要成分,则为二氧化硅,硅元素的质量为![]() =5.6g,根据逆分析法可知,A中含硅元素,又为氢化物,则推出A为SiH4;固体E为耐高温材料,根据逆推法结合过量氢氧化钠溶液可知,该耐高温材料不是氧化铝,而应为氧化镁,镁元素的质量为
=5.6g,根据逆分析法可知,A中含硅元素,又为氢化物,则推出A为SiH4;固体E为耐高温材料,根据逆推法结合过量氢氧化钠溶液可知,该耐高温材料不是氧化铝,而应为氧化镁,镁元素的质量为![]() =9.6g,白色沉淀为氢氧化镁,溶液C为硫酸镁溶液,根据元素守恒可知,固体X含镁与硅元素,且原子个数比为
=9.6g,白色沉淀为氢氧化镁,溶液C为硫酸镁溶液,根据元素守恒可知,固体X含镁与硅元素,且原子个数比为![]() :
:![]() =2:1,应为Mg2Si,据此分析作答。
=2:1,应为Mg2Si,据此分析作答。
(1)依据上述分析可知,固体X为Mg2Si,
故答案为:Mg2Si;
(2)C→D是硫酸镁与过量氢氧化钠反应生成氢氧化镁的过程,其离子方程式为:
Mg2+ + 2OH- == Mg(OH)2↓,
故答案为:Mg2+ + 2OH- == Mg(OH)2↓;
(3)NH3与SiH4在一定条件下反应后可得到的一种耐高温材料中含N与Si,仅含两种元素,摩尔质量为140 g·mol-1,则该化合物为Si3N4和H2,其化学方程式为:3SiH4+4NH3== Si3N4+12H2↑,
故答案为:3SiH4+4NH3== Si3N4+12H2↑。

练习册系列答案
 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案 名校提分一卷通系列答案
名校提分一卷通系列答案
相关题目