题目内容
19.用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )| A. | 常温常压下,6gO2和26gO3混合气体中的原子总数为2NA | |
| B. | 100mL 0.1mol/L的NaCl溶液中,所含微粒总数为0.02NA | |
| C. | 23g金属钠变为钠离子时得到的电子数为NA | |
| D. | 标准状况下,2.24LH2O所含的原子数为0.3NA |
分析 A、氧气和臭氧均由氧原子构成;
B、氯化钠溶液中,微粒包括离子、分子、原子等,所以必须指明具体的粒子名称;
C、金属单质只能失电子;
D、标况下,水为液体.
解答 解:A、氧气和臭氧均由氧原子构成,故32g混合气体中含有的氧原子的物质的量n=$\frac{32g}{16g/mol}$=2mol,即为2NA个,与氧气和臭氧的质量分别是多少无关,故A正确;
B、100mL 0.1mol/L的NaCl中含有溶质氯化钠0.01mol,题中没有告诉具体的粒子名称,无法计算溶液中含有的微粒数目,故B错误;
C、由于金属元素无负价,故金属单质只能失电子,不能得电子,故C错误;
D、标况下,水为液体,故不能根据气体摩尔体积来计算其物质的量,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,熟练掌握公式的运用和物质的结构是解题关键.

练习册系列答案
相关题目
9.把100mL含有MgSO4和K2SO4的混合溶液分成二等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡.则原混合溶液中钾离子的浓度为( )
| A. | 20(2b-a) mol/L | B. | 20(b-2a) mol/L | C. | 10(2b-a) mol/L | D. | 10(b-2a) mol/L |
10.铁、铜混合粉末18.0g加人到100m1 5.0mol/L FeC13溶液中,剩余固体质量为3.2g,下列说法正确的是( )
| A. | 剩余固体是铁、铜混合物 | |
| B. | 原固体混合物中铜的质量是6.4g | |
| C. | 反应后溶液中n(Fe3十)=0.l0mol | |
| D. | 反应后溶液中n(Fe2十)+n(Cu2十)=0.75mo1 |
7.下列物质属于弱电解质的是( )
| A. | 金属钠 | B. | 硫酸 | C. | 次氯酸 | D. | 氯酸钾 |
14.某有机物的结构简式如图所示,有关该有机物的叙述正确的是( )


| A. | 分子中含有3 种官能团 | |
| B. | 在一定条件下,能发生取代、氧化、酯化和加聚反应 | |
| C. | 该物质分子中最多可以有10 个碳原子在同一平面上 | |
| D. | 1 mol 该物质最多可与5 mol H2发生加成反应 |
4.据报道,科学家通过对稻壳进行控制性焚烧热解,从中提取一种叫做生物质纳米结构二氧化硅的超高活性材料,将少量这种材料掺入混凝土中,即可制备出超高强度的高性能混凝土.下列关于二氧化硅的说法中,正确的是( )
| A. | 二氧化硅溶于水显酸性,所以二氧化硅属于酸性氧化物 | |
| B. | 将二氧化碳通入硅酸钠溶液可以得到硅酸 | |
| C. | 因为高温时二氧化硅与碳酸钠反应放出二氧化碳,所以硅酸的酸性比碳酸强 | |
| D. | 二氧化硅是酸性氧化物,它不溶于任何酸 |
11.下列说法不正确的是( )
| A. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA | |
| B. | 常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA | |
| C. | 18g H2O含有10NA个质子 | |
| D. | 1mol K2SO4中阴离子所带电荷数为NA |
8.用NA表示阿伏加德罗常数的值,下列说法不正确的是( )
| A. | 1molNaC1中阴、阳离子数之和为2NA | B. | 0.3mol NH3中所含质子数为3NA | ||
| C. | 0.2molNa2SO4所带电荷数为0.2NA | D. | 2mol HNO3中所含原子数为10NA |
1.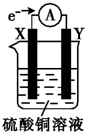 将用导线连接的电极X、Y插入装有硫酸铜溶液的烧杯中(外电路中电子流向如图所示).据此判断下列说法正确的是( )
将用导线连接的电极X、Y插入装有硫酸铜溶液的烧杯中(外电路中电子流向如图所示).据此判断下列说法正确的是( )
 将用导线连接的电极X、Y插入装有硫酸铜溶液的烧杯中(外电路中电子流向如图所示).据此判断下列说法正确的是( )
将用导线连接的电极X、Y插入装有硫酸铜溶液的烧杯中(外电路中电子流向如图所示).据此判断下列说法正确的是( )| A. | 外电路中电流方向为X→Y | |
| B. | 若电极材料分别为锌片和铜片,则Y为锌片 | |
| C. | X极上发生还原反应 | |
| D. | 若电极材料都是金属,则金属活动性:X>Y |