题目内容
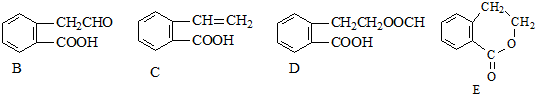
12.有机物A的结构简式为 ,它可通过不同化学反应分别制得如图B、C、D和E四种物质.
,它可通过不同化学反应分别制得如图B、C、D和E四种物质.请回答下列问题:
(1)在A~E五种物质中,互为同分异构体的是C和E(填代号).
(2)写出下列反应的化学方程式和反应类型
A→B:
 ,反应类型:氧化反应
,反应类型:氧化反应A→D:
 +HCOOH$→_{△}^{浓硫酸}$
+HCOOH$→_{△}^{浓硫酸}$ +H2O,反应类型:酯化反应或取代反应
+H2O,反应类型:酯化反应或取代反应(3)上述分子中既能发生银镜反应,又能发生水解反应的物质是C(填序号).
(4)C通过加聚反应能形成高聚物,该高聚物的结构简式为
 .
.
分析 (1)具有相同分子式、不同结构的有机物互为同分异构体,据此进行判断;
(2)A→B:A中含有-HO,可被氧化为-CHO,据此写出反应的化学方程式;
A→D: 与HCOOH发生酯化反应生成D
与HCOOH发生酯化反应生成D ,据此写出反应方程式;
,据此写出反应方程式;
(3)上述分子中既能发生银镜反应,又能发生水解反应,该物质分子中含有醛基和酯基;
(4)C中含有C=C,可发生加聚反应生成高聚物.
解答 解:(1)对比以上五种物质,C和E的分子式相同,都为C9H8O2,但结构不同,属于同分异构体,
故答案为:C和E;
(2)A→B:A中含有-HO,可被氧化为-CHO,反应的方程式为 ;
;
A→D: 与HCOOH发生酯化反应生成D
与HCOOH发生酯化反应生成D ,反应方程式为:
,反应方程式为: +HCOOH$→_{△}^{浓硫酸}$
+HCOOH$→_{△}^{浓硫酸}$ +H2O,该反应为酯化反应或取代反应,
+H2O,该反应为酯化反应或取代反应,
故答案为: ;氧化反应;
;氧化反应; +HCOOH$→_{△}^{浓硫酸}$
+HCOOH$→_{△}^{浓硫酸}$ +H2O;酯化反应或取代反应;
+H2O;酯化反应或取代反应;
(3)上述分子中既能发生银镜反应,又能发生水解反应,该物质分子中含有醛基和酯基,满足条件的为C,
故答案为:C;
(4)C中含有C=C,可发生加聚反应,该反应的方程式为: ,生成高聚物的结构简式为:
,生成高聚物的结构简式为: ,
,
故答案为: .
.
点评 本题考查有机物的结构和性质,题目难度中等,解答本题一定要注意官能团的变化,结合官能团的性质判断有机物可能具有的性质,试题侧重考查学生的分析、理解能力及灵活应用能力.

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
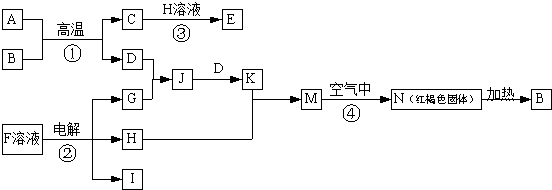
2.已知2A(g)+B(g)?2C(g)△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2mol A和1mol B,在500℃时充分反应达平衡后C的浓度为w mol/L,放出热量为b kJ.
(1)下表为不同温度下该反应的平衡常数.由此可推知,表中T1<T2(填“>”“=”或“<”).
若在原来的容器中,只加入2mol C,500℃时充分反应达平衡后,吸收热量为c kJ,C的浓度=(填“>”、“=”或“<”)w mol/L,a、b、c之间满足何种关系a=b+c(用代数式表示).
(2)在相同条件下要想得到2a kJ热量,加入各物质的物质的量可能是D.
A.4mol A和2mol B B.4mol A、2mol B和2mol C
C.4mol A和4mol B D.6mol A和4mol B
(3)为使该反应的反应速率增大,且平衡向正反应方向移动的是C.
A.及时分离出C气体 B.适当升高温度C.增大B的浓度 D.选择高效催化剂
(4)若将上述容器改为恒压容器(反应前体积相同),起始时加入2mol A和1mol B,500℃时充分反应达平衡后,放出热量为d kJ,则d>b(填“>”“=”或“<”).
(5)在一定温度下,向一个容积可变的容器中,通入3mol A和2mol B及固体催化剂,使之反应,平衡时容器内气体压强为起始时的90%.保持同一反应温度,在相同容器中,将起始物质的量改为4mol A、3mol B和2mol C,则平衡时A的百分含量不变(填“不变”“变大”“变小”或“无法确定”).
(1)下表为不同温度下该反应的平衡常数.由此可推知,表中T1<T2(填“>”“=”或“<”).
| T/K | T1 | T2 | T3 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
(2)在相同条件下要想得到2a kJ热量,加入各物质的物质的量可能是D.
A.4mol A和2mol B B.4mol A、2mol B和2mol C
C.4mol A和4mol B D.6mol A和4mol B
(3)为使该反应的反应速率增大,且平衡向正反应方向移动的是C.
A.及时分离出C气体 B.适当升高温度C.增大B的浓度 D.选择高效催化剂
(4)若将上述容器改为恒压容器(反应前体积相同),起始时加入2mol A和1mol B,500℃时充分反应达平衡后,放出热量为d kJ,则d>b(填“>”“=”或“<”).
(5)在一定温度下,向一个容积可变的容器中,通入3mol A和2mol B及固体催化剂,使之反应,平衡时容器内气体压强为起始时的90%.保持同一反应温度,在相同容器中,将起始物质的量改为4mol A、3mol B和2mol C,则平衡时A的百分含量不变(填“不变”“变大”“变小”或“无法确定”).
7.某物质中可能有甲酸、乙酸、甲醇和甲酸乙酯四种物质中的一种或几种.在鉴定时有下列现象:①有银镜反应;②加入新制的Cu(OH)2 悬浊液后未发现变澄清;③与含酚酞的NaOH溶液共热,红色逐渐消失.下列结论正确的是( )
| A. | 有甲酸乙酯,可能有甲醇 | B. | 有甲酸乙酯和甲酸 | ||
| C. | 有甲酸乙酯和甲醇 | D. | 几种物质均存在 |
17.已知KIO3是食用碘盐的碘添加剂,其制备原理之一为:I2+2KClO3$\frac{\underline{\;873K\;}}{\;}$Cl2+2KIO3,下列说法正确的是( )
| A. | 反应过程中I2置换出Cl2,由此可推断非金属性I>Cl | |
| B. | 反应中I2为氧化剂,Cl2为氧化产物 | |
| C. | 生成1 mol Cl2时转移2 mol电子 | |
| D. | 由方程式可知还原性I2>Cl2 |
1.分子式为C4H802的酯共有(不考虑立体异构)( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
17.下列说法错误的是( )
| A. | 淀粉水解的最终产物能发生银镜反应 | |
| B. | 纤维素由葡萄糖分子缩合而成,能表现出多元醇的性质 | |
| C. | 蛋白质的水溶液加入铜盐,可以发生盐析 | |
| D. | 天然蛋白质水解最终产物都是α-氨基酸 |
 .
.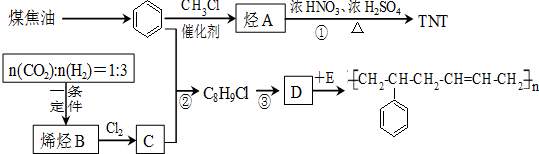
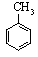 +3HNO3$→_{△}^{浓硫酸}$
+3HNO3$→_{△}^{浓硫酸}$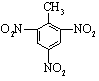 +3H2O.
+3H2O.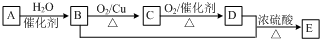
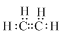 ;欲鉴别A与甲烷可选择溴水或酸性高锰酸钾溶液作试剂.
;欲鉴别A与甲烷可选择溴水或酸性高锰酸钾溶液作试剂.