题目内容
【题目】在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g)![]() N2O4(g),如图所示。
N2O4(g),如图所示。
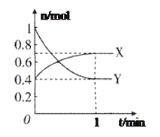
(1)曲线__(填“X”或“Y”)表示NO2的物质的量随时间的变化曲线。
(2)在0到1min中内用X表示该反应的速率是__,该反应达限度时,Y的转化率是__。
(3)下列能说明该反应已达到化学平衡状态的是__。(填标号)。
A.v(NO2)=2v(N2O4)
B.容器内压强不再发生变化
C.容器内分子总数不再发生变化
D.容器内N2O4与NO2物质的量相同
E.消耗nmolN2O4的同时生成2nmolNO2
【答案】Y 0.15mol·L-1·min-1 60% BC
【解析】
根据化学计量数,可知NO2的变化量是N2O4的变化量的2倍,从图可知,Y的物质的量从1mol降低到0.4mol变化了0.6mol,X的物质的量从0.4mol增加到0.7mol变化了0.3mol,可知Y表示的是NO2,X表示的N2O4。
(1)根据化学计量数,可知NO2的变化量是N2O4的变化量的2倍,从图可知,Y的物质的量从1mol降低到0.4mol变化了0.6mol,X的物质的量从0.4mol增加到0.7mol变化了0.3mol,可知Y表示的是NO2,X表示的N2O4。则Y表示的NO2的物质的量随时间的变化曲线;
(2)X表示N2O4,其物质的量在0-1min中内从0.4mol增加到0.7mol,则表示的化学反应速率是![]() ;
;
Y表示NO2,其物质的量从1mol降低到0.4mol变化了0.6mol,转化率![]() ;
;
(3)A.v(NO2)=2v(N2O4),不知道其表示的是正反应速率,还是逆反应速率,无法判断正逆反应速率是否相等,则不能说明反应已达到平衡状态,A不符合题意;
B.恒温恒容下,压强之比等于物质的量之比,该反应前后气体的物质的量发生改变,则压强发生改变,若压强不变时,则气体的物质的量不变,说明反应达到平衡状态,B符合题意;
C.分子总数和总的物质的量成正比,分子总数不变,则总物质的量不变,该反应前后气体的物质的量发生变化,则当总物质的量不变时,反应达到平衡,C符合题意;
D.达到平衡时,各物质的物质的量不变,但是不能确定NO2和N2O4的物质的量是否相等,D不符合题意;
E.消耗N2O4表示的为逆反应速率,生成NO2表示的也为逆反应速率,不能判断正逆反应速率相等,则不能判断反应是否达到平衡,E不符合题意;
综上答案选BC。

 习题精选系列答案
习题精选系列答案【题目】下列生产或实验事实引出的相应结论不正确的是( )
选项 | 事实 | 结论 |
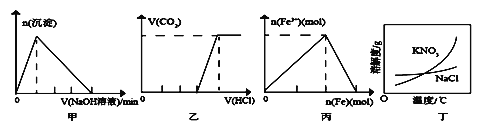
A | 其他条件相同,Na2S2O3溶液和H2SO4溶液反应,升高溶液的温度,析出硫沉淀所需时间变短 | 当其他条件不变时,升高反应温度,化学反应速率加快 |
B | 工业制硫酸中,在SO3的吸收阶段,吸收塔里要装填瓷环 | 增大气液接触面积,使SO3的吸收速率增大 |
C | 在容积可变的密闭容器中发生反应:2NH3(g) | 正反应速率加快,逆反应速率减慢 |
D | A、B两支试管中分别加入等体积5%的H2O2,在B试管中加入2~3滴FeCl3溶液,B试管中产生气泡快 | 当其他条件不变时,催化剂可以改变化学反应速率 |
A. A B. B C. C D. D
【题目】下表是A、B、C、D、E五种短周期元素的某些性质,下列判断正确的是( )
元素 | A | B | C | D | E |
最低化合价 | -4 | -2 | -1 | -2 | -1 |
电负性 | 2.5 | 2.5 | 3.0 | 3.5 | 4.0 |
A.C、D、E的简单氢化物的稳定性:C>D>E
B.元素A的原子最外层中无自旋状态相同的电子
C.元素B、C之间不可能形成化合物
D.与元素B同周期且在该周期中第一电离能最小的元素的单质能与![]() 发生置换反应
发生置换反应
【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
苯 | 溴 | 溴苯 | |
密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
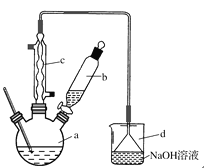
按下列合成步骤回答问题:
(1)在a中加入15 mL无水苯和少量铁屑。由b向a中加入4 mL液溴。烧瓶a中发生反应的化学方程式是______。装置d的作用是_________________;装置c的作用是__________________。
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10 mL水,然后过滤除去未反应的铁屑;
②滤液依次用10 mL水、8 mL 10%的NaOH溶液、10 mL水洗涤。NaOH溶液洗涤的作用是________________________;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是____________。
(3)经过上述分离操作后,粗溴苯中还含有的主要杂质的名称是________,进一步提纯操作方法是________。
(4)在该实验中,a的容积最适合的是________(填字母)。
A.25 mL B.50 mL C.250 mL D.500 mL
【题目】减少二氧化碳的排放,氮氧化物、二氧化硫的处理与利用是一项重要的热点课题.
Ⅰ![]() 经催化加氢可合成低碳烯烃:
经催化加氢可合成低碳烯烃:![]() 在
在![]() 时,按
时,按![]() :
:![]() :3投料,图1所示不同温度
:3投料,图1所示不同温度![]() 下,平衡时的四种气态物质的物质的量
下,平衡时的四种气态物质的物质的量![]() 的关系.
的关系.
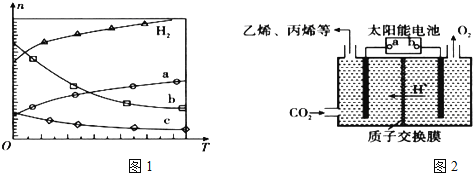
![]() 该反应的
该反应的![]() ______
______ ![]() 填“
填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]() .
.
![]() 曲线b表示的物质为 ______ .
曲线b表示的物质为 ______ .
![]() 为提高
为提高![]() 的平衡转化率,除改变温度外,还可采取的措施是 ______ .
的平衡转化率,除改变温度外,还可采取的措施是 ______ .
(2)在强酸性的电解质水溶液中,惰性材料做电极,电解![]() 可得到多种燃料,其原理如图2所示.
可得到多种燃料,其原理如图2所示.
b为电源的 ______ 极,电解时,生成乙烯的电极反应式是 ______ .
Ⅱ![]() (3)用活性炭还原法可以处理氮氧化物.如反应:
(3)用活性炭还原法可以处理氮氧化物.如反应:![]()
![]() . 在
. 在![]() 时,反应进行到不同时间测得各物质的浓度如下:
时,反应进行到不同时间测得各物质的浓度如下:
时间 浓度 | 0 | 10 | 20 | 30 | 40 | 50 |
NO |
|
|
|
|
|
|
| 0 |
|
|
|
|
|
| 0 |
|
|
|
|
|
![]() 时,该反应的平衡常数
时,该反应的平衡常数![]() ______ .
______ .
![]() 后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是 ______
后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是 ______ ![]() 答一种即可
答一种即可![]() .
.
Ⅲ.(4)工业上可以用NaOH溶液或氨水吸收过量的![]() ,分别生成
,分别生成![]() 、
、![]() ,其水溶液均呈酸性.相同条件下,同浓度的两种酸式盐的水溶液中
,其水溶液均呈酸性.相同条件下,同浓度的两种酸式盐的水溶液中![]() 较小的是 ______ ,用文字和化学用语解释原因 ______ .
较小的是 ______ ,用文字和化学用语解释原因 ______ .