题目内容
11.下列各项中所列举的物质与所属类别对应不正确的是( )| A. | 酸性氧化物:CO2、SO2、SiO2、Cl2O7 | |
| B. | 混合物:铝热剂、纯净矿泉水、水玻璃、焦炉气 | |
| C. | 同素异形体:石墨与金刚石、氧气与臭氧 | |
| D. | 非电解质:蔗糖、四氯化碳、氨气、氯气 |
分析 根据物质的组成来分析物质的类别,酸性氧化物是能与碱反应生成盐和水的化合物;非电解质是在水溶液中和熔融状态下都不导电的化合物;同素异形体是同种元素形成的不同单质;混合物是由两种或多种物质组成的,据此判断.
解答 解:A、CO2,SO2,SiO2,Cl2O7都是能与碱反应生成盐和水的化合物,属于酸性氧化物,故A正确;
B、铝热剂,纯净矿泉水,水玻璃,焦炉气均是由两种或多种物质组成的,属于混合物,故B正确;
C、活性炭,C60,石墨,金刚石都是碳元素的不同单质,属于同素异形体,氧气与臭氧,都是氧元素的不同单质,属于同素异形体,故C正确;
D、非电解质是在水溶液中和熔融状态下都不导电的化合物,氯气是单质,不是非电解质,故D错误;
故选D.
点评 本题难度不大,考查物质类别的判别,抓住酸性氧化物、非电解质、同素异形体、混合物的概念,熟悉常见的物质的组成是正确解答本题的关键.

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
1.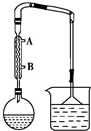 某课外兴趣小组以正丁醇为主要原料,利用图示装置制备1-溴丁烷.实验过程如下:
某课外兴趣小组以正丁醇为主要原料,利用图示装置制备1-溴丁烷.实验过程如下:
Ⅰ制备:圆底烧瓶中依次加入5mL水、5mL浓硫酸、3.1mL正丁醇和4.2g NaBr,按如图安装反应装置,用小火加热混合物至沸腾,保持回流30min,在此过程中要不断摇动反应瓶;
Ⅱ分离:移去热源,稍冷后拆去回流装置,把装置改成普通蒸馏装置,接着进行蒸馏操作,得到粗产品;
Ⅲ提纯:粗产品经洗涤、干燥、蒸馏等操作,得到产品.
回答下列问题:
(1)制备装置中冷凝管的作用是冷凝回流、导气,冷凝水的进水口为B(填“A”或“B”).
(2)加热回流后,反应瓶中的物料呈红棕色,其原因是2HBr+H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Br2↑+SO2↑+2H2O(用化学方程式表示).
(3)在制备1-溴丁烷时不能边反应边蒸出产物,其原因是1-溴丁烷与正丁醇的沸点差较小,若边反应边蒸出产物,会有较多的正丁醇挥发,降低原料的利用率.
(4)要除去1-溴丁烷中含有的少量杂质Br2,下列物质中最适合的是C.
A.NaCl B.NaOH C.NaHSO3 D.KCl.
 某课外兴趣小组以正丁醇为主要原料,利用图示装置制备1-溴丁烷.实验过程如下:
某课外兴趣小组以正丁醇为主要原料,利用图示装置制备1-溴丁烷.实验过程如下:Ⅰ制备:圆底烧瓶中依次加入5mL水、5mL浓硫酸、3.1mL正丁醇和4.2g NaBr,按如图安装反应装置,用小火加热混合物至沸腾,保持回流30min,在此过程中要不断摇动反应瓶;
Ⅱ分离:移去热源,稍冷后拆去回流装置,把装置改成普通蒸馏装置,接着进行蒸馏操作,得到粗产品;
Ⅲ提纯:粗产品经洗涤、干燥、蒸馏等操作,得到产品.
| 物质 | 颜色、状态 | 沸点(℃) | 密度(g•mL-1) | 水溶性 |
| 正丁醇 | 无色液体 | 117.2 | 0.8098 | 易溶 |
| 1-溴丁烷 | 无色液体 | 101.6 | 1.2758 | 难溶 |
(1)制备装置中冷凝管的作用是冷凝回流、导气,冷凝水的进水口为B(填“A”或“B”).
(2)加热回流后,反应瓶中的物料呈红棕色,其原因是2HBr+H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Br2↑+SO2↑+2H2O(用化学方程式表示).
(3)在制备1-溴丁烷时不能边反应边蒸出产物,其原因是1-溴丁烷与正丁醇的沸点差较小,若边反应边蒸出产物,会有较多的正丁醇挥发,降低原料的利用率.
(4)要除去1-溴丁烷中含有的少量杂质Br2,下列物质中最适合的是C.
A.NaCl B.NaOH C.NaHSO3 D.KCl.
19.下列说法中正确的是( )
| A. | 3p2表示3p能级有两个轨道 | |
| B. | M能层中的原子轨道数目为3 | |
| C. | 1s22s12p1表示的是激发态原子的电子排布 | |
| D. | 处于同一轨道上的电子可以有多个,它的运动状态完全相同 |
6.一定条件下,建立平衡2NO2(g)?N2O4(g),以下说法正确的是( )
| A. | 恒温恒容,再充入NO2,达到新平衡时,NO2的体积分数增大 | |
| B. | 恒温恒容,再充入N2,达到新平衡时,容器内颜色变浅 | |
| C. | 恒温恒容,再充入N2O4,达到新平衡时,混合气体的平均相对分子质量增大 | |
| D. | 恒温恒压,再充入Ar,达到新平衡时,NO2的转化率降低 |
16.下列各项操作中不发生先沉淀后溶解现象的是( )
①向饱和碳酸钠溶液中通入过量的CO2
②向Fe(OH)3胶体中逐滴滴加入过量H2SO4
③向Ba(NO3)2溶液中通入过量SO2
④向石灰水中通入过量CO2
⑤向硅酸钠溶液中逐滴加入过量的盐酸.
①向饱和碳酸钠溶液中通入过量的CO2
②向Fe(OH)3胶体中逐滴滴加入过量H2SO4
③向Ba(NO3)2溶液中通入过量SO2
④向石灰水中通入过量CO2
⑤向硅酸钠溶液中逐滴加入过量的盐酸.
| A. | ①②③ | B. | ①②⑤ | C. | ①②③⑤ | D. | ①③⑤ |
3.下列物质中所含分子物质的量最多的是( )
| A. | 4℃时2.7 mL 水 | |
| B. | 6.02×1022个氯化氢分子 | |
| C. | 4.9 g 磷酸 | |
| D. | 2.24 L(标准状况)一氧化碳和二氧化碳的混合气体 |
20.下列溶液中微粒的物质的量浓度关系一定正确的是( )
| A. | 0.1mol/LNH4Cl溶液与0.05mol/LNaOH溶液等体积混合后所得的碱性溶液中:c(Cl-)>c(Na+)>c(NH4+)>c(OH-)>c(H+) | |
| B. | pH=2的HA溶液与pH=12的MOH溶液等体积混合:c(M+)=c(A-)>c(OH-)=c(H+) | |
| C. | 等物质的量NaClO、NaHCO3混合溶液:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-) | |
| D. | 某二元弱酸的酸式盐NaHA溶液:c(Na+)+c(H+)=c(OH-)+c(HA-)+c(A2-) |
 ;
;