题目内容
【题目】工业上通常以2异丙基苯酚(A)为原料,生产一种常用的农药——扑灭威(B),过程如下:

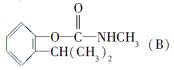
下列有关说法错误的是( )
A.上述反应属于取代反应
B.B在强酸、强碱性环境中都不能稳定存在
C.A与B可用FeCl3溶液进行鉴别
D.1molB在NaOH溶液中水解,最多消耗2molNaOH
【答案】D
【解析】
A. 根据A与B两种物质结构的差异分析;
B. B物质中存在酯基和肽键,在酸性或碱性条件下均可发生水解反应;
C. 酚类物质遇到FeCl3溶液显紫色;
D. -COO-、-CONH-以及水解生成的酚羟基均可与碱发生反应。
A. A中酚羟基变为了B中的![]() ,即-OH中的氢原子被
,即-OH中的氢原子被![]() 替代,因此发生了取代反应,A项正确,不符合题意;
替代,因此发生了取代反应,A项正确,不符合题意;
B. B物质中存在酯基和肽键,在酸性或碱性条件下均可发生水解反应,因此B在强酸、强碱性环境中都不能稳定存在,B项正确,不符合题意;
C. 酚类物质遇到FeCl3溶液显紫色,A中含有酚羟基,B中不含酚羟基,因此可以用FeCl3溶液进行鉴别,C项正确,不符合题意;
D. -COO-、-CONH-以及水解生成的酚羟基均可与碱发生反应,因此1molB在NaOH溶液中水解,可以消耗3molNaOH,D项错误,符合题意;
答案选D。

练习册系列答案
相关题目