题目内容
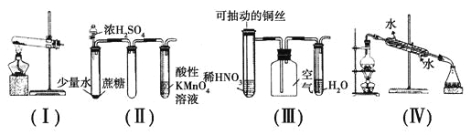
【题目】某同学研究铝及其化合物的性质时设计了如下两个实验方案:
方案①:2.7 g Al![]() X溶液
X溶液![]() Al(OH)3沉淀
Al(OH)3沉淀
方案②:2.7 g Al![]() Y溶液
Y溶液![]() Al(OH)3沉淀
Al(OH)3沉淀
NaOH溶液和稀盐酸的浓度均是3 mol·L-1,如图是向X溶液和Y溶液中分别加入NaOH溶液或稀盐酸时产生沉淀的物质的量与加入盐酸或氢氧化钠溶液体积之间的关系。下列说法正确的是( )
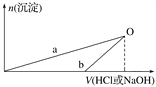
A. X溶液溶质为AlCl3,Y溶液溶质为NaAlO2
B. b曲线表示的是向X溶液中加入NaOH溶液
C. 在O点时两方案中所得溶液浓度相等
D. a、b曲线表示的反应都是氧化还原反应
【答案】C
【解析】试题分析:A、n(Al)="0.1" mol,n(HCl)="3" mol/L×0.1 L="0.3" mol,n(NaOH)="3" mol/L×0.1 L="0.3" mol,根据反应:2Al+6HCl=2AlCl3+3H2↑,2Al+2NaOH+2H2O=2NaAlO2+3H2↑可知,X为AlCl3溶液,Y为NaAlO2和NaOH的混合液,A错误;B、根据以上分析可知图象中a表示X溶液中加入的是NaOH溶液,B错误;C、在O点时,沉淀达到最大,所得溶液中只有氯化钠溶质,与向X溶液和Y溶液中分别加入NaOH和HCl的浓度及体积相等,根据原子守恒,O点时两方案中所得溶液浓度相等,C正确;D、a表示的是氯化铝和氢氧化钠的复分解反应,b表示的是偏铝酸钠和盐酸的反应,二反应不存在化合价的变化,均不属于氧化还原反应,D错误,答案选C。

【题目】已知酸性条件下有以下反应关系: ①KBrO3能将KI氧化成I2或KIO3,其本身被还原为Br2。②Br2能将I-氧化为I2。③KIO3能将I-氧化为I2,也能将Br-氧化为Br2,其本身被还原为I2。现向含有1 mol KI的硫酸溶液中加入含amol KBrO3的溶液,a的取值不同,所得产物也不同。下列判断正确的是:
编号 | a的取值范围 | 产物的化学式 |
① | a≤1/6 | I2、Br- |
② | 1/6<a<1/5 | I2、Br-、Br2 |
③ | 1/5<a<6/5 | I2、IO3-、Br2 |
④ | a≥6/5 | IO3-、Br2 |
A. ①③④ B. ②③④ C. ①②③④ D. ①④