题目内容
【题目】下列离子方程式的书写中正确的是
A.氢氧化镁与盐酸反应:H++OH-=H2O
B.铁与盐酸反应:2Fe+6H+=2Fe3++3H2
C.氧化铝溶于稀硫酸:Al2O3+6H+=2Fe3++3H2O
D.向沸水中滴加FeCl3溶液制备Fe(OH)3 胶体:Fe3++3H2O=Fe(OH)3+3H+
【答案】C
【解析】
A. 氢氧化镁难溶物,不能拆,故A错误;
B. 铁与盐酸反应生成亚铁盐即:Fe+2H+=Fe2++H2↑,故B错误;
C. 氧化铝溶于稀硫酸反应生成硫酸铝和水,其离子反应方程式为:Al2O3+6H+=2Fe3++3H2O,故C正确;
D. 向沸水中滴加饱和的FeCl3溶液,当溶液变成红褐色时,停止滴加,即可得到Fe(OH)3 胶体:Fe3++3H2O![]() Fe(OH)3(胶体)+3H+,故D错误;
Fe(OH)3(胶体)+3H+,故D错误;
答案:C。

练习册系列答案
相关题目
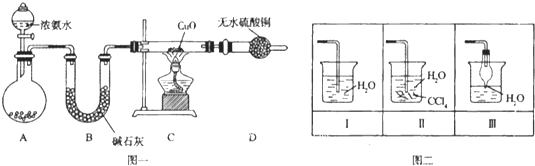
【题目】测定硫酸铜晶体(CuSO4xH2O)中x值的实验过程如下:

完成下列填空:
(1)必须要进行恒重操作的原因是___。
(2)下面是某同学的一次实验记录,请完成下表。
称量数据1 | 称量数据2 | 称量数据3 | 结晶水的X值 | 实验误差 |
11.685g | 13.691g | 12.960g | ____ | ____ |
(3)本次实验测得X值偏__(高、低),可能这次实验中产生误差的原因可能是___。
A.硫酸铜晶体中含有不挥发性杂质 B.实验前晶体表面有湿存水
C.加热时有晶体飞溅出去 D.加热失水后露置在空气中冷却