题目内容
10.可确定乙二醇分子是否有极性的实验是( )| A. | 测定沸点 | B. | 测静电对液流影响 | ||
| C. | 测定蒸气密度 | D. | 测标准状况下气体摩尔体积 |
分析 极性分子中正负电荷中心中心不重叠,作静电引流实验时会偏转,据此分析.
解答 解:极性分子的正电荷中心与负电荷中心不重合,极性分子虽然整体不带电,但每一个乙醇分子都有带电的极性端,也可以再理解为部分区域带电,所以它在电场作用下,会定向运动,所以测静电对液流影响,可以判断分子是否有极性;而测定沸点、测定蒸气密度、测标准状况下气体摩尔体积等均不能判断分子极性;
故选B.
点评 本题考查了分子极性的实验室测定方法,题目难度不大,注意把握静电引流实验的原理.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
1.如图是达到平衡后,外界条件变化时,2SO2(g)+O2(g)?2SO3(g);△H<0反应速率的变化情况(v′表示正反应速率,v″表示逆反应速率).下列说法中正确的是( )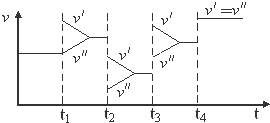

| A. | t1时改变的条件是增大体系的压强 | B. | t2时改变的条件是减小压强 | ||
| C. | t3时改变的条件是升高温度 | D. | t4时改变的条件是使用了催化剂 |
5.钛及其合金具有许多优异的性能.具有超导特性、形状记忆和吸氧特性等,而被称为“太空金属”和“海洋金属”,在航空航天、海洋开发、化工、冶金、汽车等领域有着越来越广泛的用途.
(1)Ti(BH4)2是一种过渡元素硼氢化物材料,基态钛原子外围电子构型为3d24s2;在Ti(BH4)2中钛元素化合价为+2,与Ti(BH4)2中的阴离子互为等电子体CH4.(写一种即可)
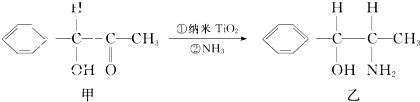
(2)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如图1所示,化合物甲的分子中采取sp2方式杂化的碳原子数为7个,化合物乙中采取sp3方式杂化的原子对应的元素的电负性由大到小的顺序为C<O<N.
(3)科学家通过X-射线探明KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似,且知三种离子晶体的晶格能数据如表:
KCl、CaO、TiN三种离子晶体熔点由高到低的顺序是为CaO>NaCl>KCl.
(4)Ti3+可形成配位数为6的配合物,现有钛的两种颜色的配合物,一种为紫色,另一种为绿色.相关实验证明,两种晶体的组成皆为TiCl3•6H2O.为测定这两种配合物的成键情况,
设计了如下实验:分别取等质量的两种物质的样品配成待测溶液,分别往待测溶液中滴入过量的AgNO3溶液并充分反应,均产生白色沉淀;测定沉淀质量并比较,发现原绿色物质得到的沉淀质量由原来紫色物质得到沉淀质量的$\frac{2}{3}$.则原绿色晶体配合物的化学式为[TiCl(H2O)5]Cl2•H2O.
(5)有一种氮化钛晶体的晶胞和氯化钠晶胞相似,如图2所示,该晶胞中N、Ti之间的最近距离为apm,则该氧化钛的密度为$\frac{62×4}{(2a×1{0}^{-10})^{3}{N}_{A}}$g/cm3(NA为阿伏伽德罗常数的数值,只列计算式).该晶体中与N原子距离相等且最近的N原子有12个.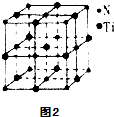
(1)Ti(BH4)2是一种过渡元素硼氢化物材料,基态钛原子外围电子构型为3d24s2;在Ti(BH4)2中钛元素化合价为+2,与Ti(BH4)2中的阴离子互为等电子体CH4.(写一种即可)
(2)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如图1所示,化合物甲的分子中采取sp2方式杂化的碳原子数为7个,化合物乙中采取sp3方式杂化的原子对应的元素的电负性由大到小的顺序为C<O<N.

(3)科学家通过X-射线探明KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似,且知三种离子晶体的晶格能数据如表:
| 晶体 | NaCl | KCl | CaO |
| 晶格能/(Kj.mol-1) | 786 | 715 | 3401 |
(4)Ti3+可形成配位数为6的配合物,现有钛的两种颜色的配合物,一种为紫色,另一种为绿色.相关实验证明,两种晶体的组成皆为TiCl3•6H2O.为测定这两种配合物的成键情况,
设计了如下实验:分别取等质量的两种物质的样品配成待测溶液,分别往待测溶液中滴入过量的AgNO3溶液并充分反应,均产生白色沉淀;测定沉淀质量并比较,发现原绿色物质得到的沉淀质量由原来紫色物质得到沉淀质量的$\frac{2}{3}$.则原绿色晶体配合物的化学式为[TiCl(H2O)5]Cl2•H2O.
(5)有一种氮化钛晶体的晶胞和氯化钠晶胞相似,如图2所示,该晶胞中N、Ti之间的最近距离为apm,则该氧化钛的密度为$\frac{62×4}{(2a×1{0}^{-10})^{3}{N}_{A}}$g/cm3(NA为阿伏伽德罗常数的数值,只列计算式).该晶体中与N原子距离相等且最近的N原子有12个.

15.为了实现绿色化学,符合工业生产实际的是( )
| A. | 用纯碱吸收硫酸工业的尾气 | B. | 用烧碱吸收氯碱工业的尾气 | ||
| C. | 用纯碱吸收合成氨工业的尾气 | D. | 用烧碱吸收炼铁工业的尾气 |
2.黄铜矿(CuFeS2)是提取铜的主要原料,其煅烧产物Cu2S在1200℃高温下继续反应:2Cu2S+3O2→2Cu2O+2SO2…①2Cu2O+Cu2S→6Cu+SO2…②.则( )
| A. | 反应①中还原产物只有SO2 | |
| B. | 反应②中Cu2S只发生了氧化反应 | |
| C. | 将1 molCu2S冶炼成 2mol Cu,需要O21mol | |
| D. | 若1molCu2S完全转化为2molCu,则转移电子数为2NA |
19.如图表示M的结构简式,下列有关M的说法正确的是( )
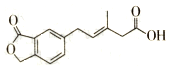

| A. | M可以发生加成、加聚、水解、酯化等反应 | |
| B. | l mol M最多可以与3 mol NaOH反应 | |
| C. | M苯环上的一氯取代物有两种不同结构 | |
| D. | l molM最多可以与5 mol H2发生加成反应 |
20.为高空或海底作业提供氧气的物质是( )
| A. | KClO3 | B. | KMnO4 | C. | Na2O2 | D. | H2O |
 .
. .
.