题目内容
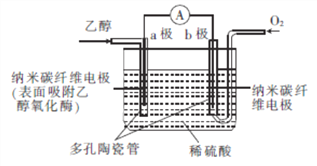
【题目】常温常压下,某生物燃料电池(BFC)以乙醇为燃料,直接或间接利用酶作催化剂,其总反应为C2H5OH+302![]() 2C02+3H20,其工作原理如图所示。下列有关说法正确的是( )
2C02+3H20,其工作原理如图所示。下列有关说法正确的是( )
A. 乙醇发生还原反应
B. b极上的电极反应式为O2+4e-+H2O=4OH-
C. 电池工作时,电解液中的H+由a极向b极迁移
D. 当外电路中有1.2 mol电子转移时,能产生4.48 L CO2
【答案】C
【解析】A.由总反应式C2H5OH+302=2C02+3H20可知乙醇发生氧化反应,故A错误;B.b极能氧气,为正极,发生还原反应,电极反应式为O2+4e-+4H+=2H2O,故B错误;C.原电电池工作时,电解液中的H+向正极移动,即由a极向b极迁移,故C正确;D.当外电路中有1.2mol电子转移时,能产生0.2molCO2,在标准状况下的体积为4.48 L,故D错误;答案为C。

练习册系列答案
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目