题目内容
6.下列各选项中的反应①与反应 ②能用同一离子方程式表示的是( )| 序号 | 反应① | 反应② |
| A | NaOH与HCl反应 | Mg(OH)2与HNO3反应 |
| B | 向BaCl2溶液中滴加稀H2SO4 | 向Ba(OH)2溶液中滴加CuSO4溶液 |
| C | Cl2通入NaOH溶液中 | Cl2通入澄清石灰水中 |
| D | Fe与HCl反应 | Fe与CH3COOH反应 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.NaOH为强碱、氢氧化镁为弱碱;
B.BaCl2溶液中滴加稀H2SO4反应生成硫酸钡沉淀,而Ba(OH)2溶液中滴加CuSO4溶液反应生成硫酸钡沉淀和氢氧化铜沉淀;
C.Cl2通入NaOH溶液反应生成氯化钠、次氯酸钠和水,Cl2通入澄清石灰水中反应生成氯化钙、次氯酸钙、水;
D.盐酸为强酸,醋酸为弱酸.
解答 解:A.离子反应分别为H++OH-=H2O、Mg(OH)2+2H+=Mg2++2H2O,所以离子方程式不同,故A不选;
B.离子反应分别Ba2++SO42-=BaSO4↓、Ba2++2OH-+SO42-+Cu2+=BaSO4↓+Cu(OH)2↓,所以离子方程式不同,故B不选;
C.离子反应均为Cl2+2OH-=Cl-+ClO-+H2O,故C选;
D.离子反应分别为Fe+2H+=Fe2++H2↑、Fe+2CH3COOH=2CH3COO-+Fe2++H2↑,故D不选;
故选C.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.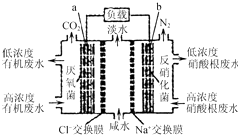 一种三室微生物燃料电池污水净化系统原理如图所示,图中有机废水中有机物可用C6H10O5表示.下列有关说法正确的是( )
一种三室微生物燃料电池污水净化系统原理如图所示,图中有机废水中有机物可用C6H10O5表示.下列有关说法正确的是( )
 一种三室微生物燃料电池污水净化系统原理如图所示,图中有机废水中有机物可用C6H10O5表示.下列有关说法正确的是( )
一种三室微生物燃料电池污水净化系统原理如图所示,图中有机废水中有机物可用C6H10O5表示.下列有关说法正确的是( )| A. | b电极为该电池的负极 | |
| B. | b电极附近溶液的pH减小 | |
| C. | a电极反应式:C6H10O5-24e-+7H2O═6CO2↑+24H+ | |
| D. | 中间室:Na+移向左室,Cl-移向右室 |
11.某同学取一定量某工厂所排废水试样,进行如下实验:
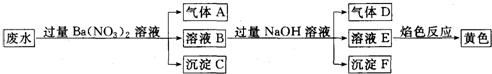
已知废水试样中可能含有下表离子中若干种.
下列判断不正确的是( )
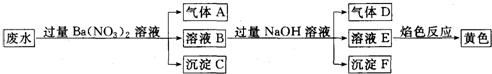
已知废水试样中可能含有下表离子中若干种.
| 阳离子 | Ba2+、K+、NH4+、Fe2+、Fe3+、X |
| 阴离子 | CO32-、SO32-、NO3-、Y |
| A. | 离子X是H+,离子Y是SO42- | |
| B. | 不能确定NO3-是否存在与废水中 | |
| C. | 沉淀C是纯净物 | |
| D. | 废水中一定存在Fe2+、NH4+,可能存在K+ |
8. 25℃时在10mL0.1mol/LNa2CO3溶液中逐滴加入0.1mol/LHCl溶液20mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示.下列说法不正确的是( )
25℃时在10mL0.1mol/LNa2CO3溶液中逐滴加入0.1mol/LHCl溶液20mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示.下列说法不正确的是( )
 25℃时在10mL0.1mol/LNa2CO3溶液中逐滴加入0.1mol/LHCl溶液20mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示.下列说法不正确的是( )
25℃时在10mL0.1mol/LNa2CO3溶液中逐滴加入0.1mol/LHCl溶液20mL,溶液中部分含碳微粒的物质的量随溶液pH的变化如图所示.下列说法不正确的是( )| A. | 当溶液的pH=8时,溶液中NaHCO3的物质的量浓度为0.1mol/L | |
| B. | HCl溶液滴加一半时,溶液pH>7 | |
| C. | 0.1mol/LNa2CO3溶液中c(Na+)+c(H+)=c(OH-)+2c(CO32-)+c(HCO3-) | |
| D. | 在M点:c(Na+)>c(CO32-)=c(HCO3-)>c(OH-)>c(H+) |
11.下列晶体中,不是六个原子构成的最小环的是( )
| A. | 金刚石 | B. | 石墨 | C. | 水晶 | D. | 晶体硅 |
18.不论以何种比例混合,将甲和乙两种混合气体同时通入过量的丙溶液中,一定能产生沉淀的组合是( )
| 序号 | 甲 | 乙 | 丙 |
| ① | CO2 | NH3 | CaCl2 |
| ② | CO2 | SO2 | 石灰水 |
| ③ | NO2 | SO2 | BaCl2 |
| ④ | HCl | CO2 | 石灰水 |
| A. | ②③④ | B. | ①②③ | C. | ①③④ | D. | 全部 |
15.将铁屑溶于过量盐酸后,再加入下列物质,不会有三价铁生成的是( )
| A. | 过氧化氢 | B. | 氯水 | C. | 硝酸锌 | D. | 氯化铜 |
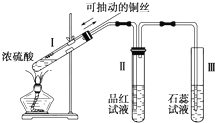 某化学兴趣小组为探究铜跟浓硫酸的反应,用如图所示装置进行有关实验.请回答:
某化学兴趣小组为探究铜跟浓硫酸的反应,用如图所示装置进行有关实验.请回答: