题目内容
美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电源,其构造如下图所示:a、b两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电。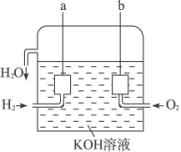
(1)a是 极,b是 极。电极反应式分别为_________________、__________________。
(2)飞船上宇航员的生活用水由燃料电池提供。已知这种电池发1度电时能生成350 g水,试计算能量的转化率。[2H2(g)+O2(g)====2H2O(l);ΔH=-572 kJ·mol-1]
(3)这种电池的输出电压为1.2 V。要使标有1.2 V、1.5 W小灯泡连续发光1 h,则消耗标准状况下的H2的体积是________L。
(1)负 正 O2+2H2O+4e-====4OH- 2H2+4OH--4e-====4H2O
(2)生成350 g水共释放化学能Q1=![]() ×572 kJ=5 561 kJ,发1度电获电能Q2=1 kW×3 600 s=3 600 kJ,转化率η=
×572 kJ=5 561 kJ,发1度电获电能Q2=1 kW×3 600 s=3 600 kJ,转化率η=![]() ×100%=
×100%=![]() ×100%=64.7%。
×100%=64.7%。
(3)灯泡耗用电能Q=1.5 W×3 600 s=5.4 kJ,需H2的物质的量
n(H2)=![]() =0.029 mol
=0.029 mol
则V(H2)=0.029 mol×22.4 L·mol-1=0.65 L
解析:由图示可知,参与电极反应的是H2和O2,生成的是H2O,故在反应中H2失去电子被氧化,a为负极;O2得到电子被还原,b为正极。

练习册系列答案
相关题目

 美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电源,其构造如图所示:a、b两个电极均由多孔碳制成,通入的气体由孔隙中逸出,并在电极表面放电.
美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电源,其构造如图所示:a、b两个电极均由多孔碳制成,通入的气体由孔隙中逸出,并在电极表面放电.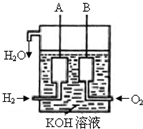 已知在25°C、1.013×105Pa下,1mol氢气完全燃烧生成液态水放出285kJ的热量,请回答下列问题:
已知在25°C、1.013×105Pa下,1mol氢气完全燃烧生成液态水放出285kJ的热量,请回答下列问题: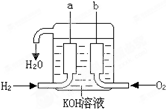 美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电源,被称为21世纪的明星电池,其构造如图所示:两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电.
美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电源,被称为21世纪的明星电池,其构造如图所示:两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电. 美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电池,其构造如图所示;两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电.
美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电池,其构造如图所示;两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电.