题目内容
在容积不变的密闭容器中,一定条件下发生反应:2A(?) B(g)+C(s),达到化学平衡后,升高温度,容器内气体的密度增大,则下列叙述正确的是
B(g)+C(s),达到化学平衡后,升高温度,容器内气体的密度增大,则下列叙述正确的是
 B(g)+C(s),达到化学平衡后,升高温度,容器内气体的密度增大,则下列叙述正确的是
B(g)+C(s),达到化学平衡后,升高温度,容器内气体的密度增大,则下列叙述正确的是 | A.若正反应是吸热反应,则A为非气态 |
| B.若正反应是放热反应,则A为非气态 |
| C.平衡体系中加入少量C,平衡向逆反应方向移动 |
| D.改变压强对该平衡的移动一定无影响 |
A
试题分析:密度是混合气的质量和容器容积的比值,在反应过程中容器容积是不变的。由于达到化学平衡后,升高温度,容器内气体的密度增大,这说明气体的质量是增加的。所以如果正反应是吸热反应,则平衡向正反应方向移动。由于C是固态,所以此时A一定不是气态,选项A正确;如果正反应是放热反应,则平衡向逆反应方向移动。由于C是固态,所以此时A一定也是气态,B不正确;改变固态的质量,不会影响平衡状态,C不正确;根据以上的讨论可知,该反应前后气体体积一定是变化的,所以改变压强对该平衡的移动一定有影响,D不正确,答案选A。
点评:影响平衡状态的外界条件一般是温度、浓度和压强。在使用时除了注意利用勒夏特例原理外,还需要特别注意体积的使用范围。例如浓度不能适用于固态或纯液态,压强只能适用于气体体系等。

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
 2NH3反应,在一定温度下达到平衡时,H2的转化率为25%。若在同一容器中在相同温度下充入NH3,欲达到平衡时各成分的百分含量与上述平衡相同,则起始时充入NH3的物质的量和达到平衡时NH3的转化率
2NH3反应,在一定温度下达到平衡时,H2的转化率为25%。若在同一容器中在相同温度下充入NH3,欲达到平衡时各成分的百分含量与上述平衡相同,则起始时充入NH3的物质的量和达到平衡时NH3的转化率 3H2(g)+N2(g),并达到平衡。则:
3H2(g)+N2(g),并达到平衡。则: 2Z,其平衡常数为1600
2Z,其平衡常数为1600 cZ(g),如图是不同温度下反应达到平衡时,反应混合物中Z的体积分数和压强的关系示意图。
cZ(g),如图是不同温度下反应达到平衡时,反应混合物中Z的体积分数和压强的关系示意图。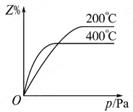
 2HI(g),已知H2和I2的起始浓度均为0.1 mol·L-1时,达平衡时HI的浓度为0.16 mol/L。若H2和I2的起始浓度均变为0. 2 mol/L,则平衡时H2的浓度是( )
2HI(g),已知H2和I2的起始浓度均为0.1 mol·L-1时,达平衡时HI的浓度为0.16 mol/L。若H2和I2的起始浓度均变为0. 2 mol/L,则平衡时H2的浓度是( ) C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下: CO2+H2;在827℃时的平衡常数是100,如果反应开始时,一氧化碳和水蒸气的浓度都是0.011mol/L,计算:一氧化碳在此反应条件下的平衡转化率。
CO2+H2;在827℃时的平衡常数是100,如果反应开始时,一氧化碳和水蒸气的浓度都是0.011mol/L,计算:一氧化碳在此反应条件下的平衡转化率。 2SO2(g)+ O2 (g)下列有关说法正确的是
2SO2(g)+ O2 (g)下列有关说法正确的是