题目内容
14.A、B、C、D均为中学化学常见的物质,它们间的反应关系如图所示.
(1)若A是可溶性强碱,B是正盐,D不溶于稀硝酸,则B的化学式为(NH4)2SO4.有关反应的化学变化的化学方程式为(NH4)2SO4+Ba(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$BaSO4↓+2NH3↑+2H2O.
(2)若B是正盐,D既可溶于盐酸又可溶于NaOH溶液.
①A是NaHCO3时,该反应的离子方程式为:Al3++3HCO3-═Al(OH)3↓+3CO2↑
②A是一种淡黄色固体,且A与B以物质的量之比3:1反应时,生成的D的量最多,推知B的化学式为:Al2(SO4)3.
(3)若A是碳化钙(CaC2),B是一种盐,A与B的溶液反应时只生成气体C、CaCO3和水;则B的化学式为Ca(HCO3)2.
分析 (1)若A是可溶性强碱,B是正盐,二者反应生成气体,应为铵盐,D不溶于稀硝酸,则A为Ba(OH)2,B为(NH4)2SO4,D为BaSO4、C为NH3;
(2)若B是正盐,D既可溶于盐酸又可溶于NaOH溶液,可推知D为氢氧化铝沉淀.
①A是NaHCO3时,应是铝离子与碳酸氢根发生水解反应反应生成氢氧化铝沉淀与二氧化碳;
②A是一种淡黄色固体,且A与B以物质的量之比3:1反应时,生成的D的量最多,即氢氧离子与铝离子为3:1,则A为Na2O2,B为 Al2(SO4)3.
(3)若A是碳化钙(CaC2),B是一种盐,A与B的溶液反应时只生成气体C、CaCO3和水,则B为Ca(HCO3)2,C为乙炔.
解答 解:(1)若A是可溶性强碱,B是正盐,二者反应生成气体,应为铵盐,D不溶于稀硝酸,则A为Ba(OH)2,B为(NH4)2SO4,D为BaSO4、C为NH3,反应方程式为:(NH4)2SO4+Ba(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$BaSO4↓+2NH3↑+2H2O,
故答案为:(NH4)2SO4;(NH4)2SO4+Ba(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$BaSO4↓+2NH3↑+2H2O;
(2)若B是正盐,D既可溶于盐酸又可溶于NaOH溶液,可推知D为氢氧化铝沉淀.
①A是NaHCO3时,应是铝离子与碳酸氢根发生水解反应反应生成氢氧化铝沉淀与二氧化碳,反应离子方程式为:Al3++3HCO3-═Al(OH)3↓+3CO2↑,
故答案为:Al3++3HCO3-═Al(OH)3↓+3CO2↑;
②A是一种淡黄色固体,且A与B以物质的量之比3:1反应时,生成的D的量最多,即氢氧离子与铝离子为3:1,则A为Na2O2,B为 Al2(SO4)3,
故答案为:Al2(SO4)3;
(3)若A是碳化钙(CaC2),B是一种盐,A与B的溶液反应时只生成气体C、CaCO3和水,则B为Ca(HCO3)2,C为乙炔,
故答案为:Ca(HCO3)2.
点评 本题考查无机物推断,需要学生熟练掌握元素化合物性质,属于猜测验证型题目,难度中等.

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案| A. | 煤的气化和液化属于物理变化 | |
| B. | 绿色化学的核心是利用化学原理从源头上减少和消除污染 | |
| C. | 淀粉、纤维素、聚乙烯都属于天然高分子化合物 | |
| D. | 金属冶炼的方法与其活泼性没有直接关系 |
| A. | 乙醇 | B. | 苯酚 | C. | 乙醛 | D. | 乙酸 |
| A. | CH4分子的比例模型: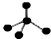 | B. | 乙醇的结构式: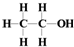 | ||
| C. | CCl4的电子式: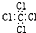 | D. | 乙醛的结构简式:CH3CHO |
| A. | 15% | B. | 30% | C. | 60% | D. | 75% |

| A. | 去甲肾上腺素分子式C8H10O3N | |
| B. | 每个去甲上腺素分子中含3个碳碳双键、3个酚羟基 | |
| C. | 1mol去甲肾上腺素最多能与2molBr2发生取代反应 | |
| D. | 去甲肾上腺素既能与盐酸反应,又能与氢氧化钠溶液反应 |
①聚乙烯塑料的老化是因为发生了加成反应
②利用粮食酿酒经历了淀粉→葡萄糖→乙醇的化学变化的过程
③淀粉、油脂、蛋白质在一定条件下都能发生水解反应
④石油的分馏和煤的干馏都是发生了化学变化
⑤淀粉遇碘酒变蓝色,葡萄糖能与新制Cu(OH)2发生反应
⑥向两份蛋白质溶液中分别滴加饱和NaCl溶液和CuSO4溶液,均有固体析出,所以蛋白质均发生盐析.
| A. | ①②③④⑤ | B. | ②③⑤ | C. | ②③④⑤ | D. | ②⑤⑥ |
| A. | 混合气体的颜色变浅 | B. | 混合气体密度变小 | ||
| C. | 混合气体的平均相对分子质量不变 | D. | N2O4的质量变小 |
 .
.