题目内容
8.下列化学方程式书写正确的是( )| A. | 乙醇催化氧化制取乙醛:CH3CH2OH+O2 $→_{△}^{催化剂}$ CH3CHO+H2O | |
| B. | 苯与浓硫酸、浓硝酸的混合液共热制硝基苯: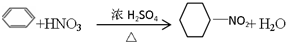 | |
| C. | 乙酸和乙醇发生反应生成乙酸乙酯:CH3CH2OH+CH3COOH$?_{△}^{催化剂}$CH3COOC2H5 | |
| D. | 乙烯使酸性高锰酸钾溶液褪色:5CH2=CH2+12 MnO4-+36H+→10CO2+12 Mn2++28H2O |
分析 A、乙醇催化氧化得到乙醛和水;
B、苯与浓硫酸、浓硝酸的混合液共热可以获得硝基苯,根据硝基苯的写法来回答判断;
C、乙酸和乙醇发生反应生成乙酸乙酯和水;
D、乙烯和酸性高锰酸钾溶液之间可以发生氧化还原反应.
解答 解:A、乙醇催化氧化得到乙醛和水,发生反应为:2CH3CH2OH+O2 $→_{△}^{催化剂}$ 2CH3CHO+2H2O,故A错误;
B、苯与浓硫酸、浓硝酸的混合液共热可以获得硝基苯,选项中生成硝基苯而不是硝基环己烷,故B错误;
C、乙酸和乙醇发生反应生成乙酸乙酯和水,反应为:CH3CH2OH+CH3COOH$?_{△}^{催化剂}$CH3COOC2H5+H2O,故C错误;
D、乙烯和酸性高锰酸钾溶液之间可以发生氧化还原反应,反应为:5CH2=CH2+12MnO4-+36H+=10CO2+12Mn2++28H2O,故D正确.
故选D.
点评 本题考查了化学方程式的书写方法和反应的原理应用,掌握物质性质和反应实质是解题关键,注意反应条件的判断,题目较简单.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
18.下列有关说法中正确的是( )
| A. | 第一电离能越大的原子越容易得到电子 | |
| B. | 同周期元素从左到右第一电离能一定增大 | |
| C. | 同周期元素电负性从左到右越来越大 | |
| D. | 金属元素的电负性一定小于非金属元素 |
16.已知短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
| A. | 原子序数:d>c>b>a | B. | 原子半径:r(A)>r(B)>r(D)>r(C) | ||
| C. | 单质的还原性:A>B>D>C | D. | 离子半径:r(C3-)>r(D-)>r(B+)>r(A2+) |
13.在下列分子结构中,有原子的最外层电子不能满足8电子稳定结构的是( )
| A. | N2 | B. | PCl3 | C. | PCl5 | D. | CO2 |
20.常温下,某无色溶液能与铝反应放出氢气,该溶液中一定能大量存在的离子组是( )
| A. | Na+、K+、MnO4-、SO42- | B. | Mg2+、NH4+、SO42-、Cl- | ||
| C. | Na+、Cl-、K+、SO42- | D. | Na+、K+、CO32-、NO3- |
 短周期元素Q、R、T、W在元素周期表中的位置如图:其中T所处的周期序数与主族序数相等,请回答下列问题
短周期元素Q、R、T、W在元素周期表中的位置如图:其中T所处的周期序数与主族序数相等,请回答下列问题 ②CH3CH2CH(CH3)CH3 ③CH4 ④
②CH3CH2CH(CH3)CH3 ③CH4 ④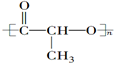 ⑤
⑤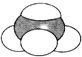 ⑥
⑥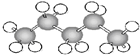 ⑦
⑦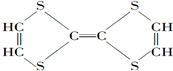

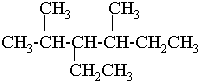
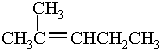 .
.