题目内容
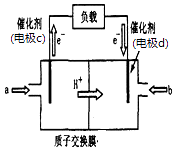
【题目】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
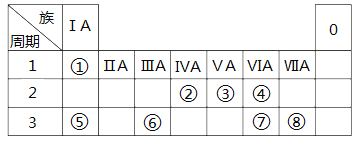
(1)写出⑥元素的名称:______________。
(2)在以上元素的原子中,原子半径最大的是___________________(填元素符号)。
(3)地壳中含量居于第二位的元素位于元素周期表中的第___________周期,第_________族。
(4)⑦元素的气态氢化物化学式为___________________。
(5)⑤元素的最高价氧化物对应的水化物化学式为______________________。
【答案】 铝 Na 三 IVA H2S NaOH
【解析】首先根据元素在周期表中的相对位置判断出元素名称,然后结合元素周期律分析解答。
参照元素①~⑧在表中的位置可知分别是H、C、N、O、Na、Al、S、Cl。则
(1)⑥元素的名称为铝。
(2)同周期自左向右原子半径逐渐减小,同主族从上到下原子半径逐渐增大,则在以上元素的原子中,原子半径最大的是Na。
(3)地壳中含量居于第二位的元素是Si,位于元素周期表中的第三周期第IVA族。
(4)硫元素的最低价是-2价,则其气态氢化物化学式为H2S。
(5)钠元素的最高价氧化物对应的水化物化学式为NaOH。

练习册系列答案
相关题目