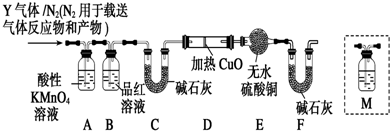
题目内容
4.用氯化钠固体配制1.00mol/L的NaCl溶液450mL,回答下列问题(1)请写出该实验的实验步骤
①计算所需NaCl的质量为29.3g,②称量,③溶解并冷却,④移液,⑤洗涤,⑥定容,⑦摇匀.
(2)所需主要仪器为:托盘天平、烧杯、玻璃棒、胶头滴管和500mL容量瓶.使用容量瓶前必须进行的操作是查漏.
(3)下列操作会使配得的溶液浓度偏小的是BE
A.容量瓶中原有少量蒸馏水
B.溶液从烧杯转移到容量瓶中后没有洗涤烧杯
C.定容时观察液面俯视
D.滴管加水时,有少量水滴到容量瓶外
E.定容摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度.
(4)某同学从该溶液中取出50ml,其中NaCl的物质的量浓度为1.00mol/L.
分析 (1)依据m=CVM计算溶质的质量,根据用固体配制溶液的一般步骤为计算、称量、溶解转移、洗涤转移、定容摇匀,据此解答;
(2)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶来分析需要的仪器;容量瓶使用前要查漏;
(3)根据c=$\frac{n}{V}$并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析;
(4)溶液是均一稳定的,取出一部分氯化钠溶液对其浓度无影响.
解答 解:(1)由于实验室无450mL容量瓶,故应选择500mL的容量瓶,故配制出500mL溶液.配制1.00mol/L的NaCl溶液0.5L,需要溶质的质量m=1.00mol/L×0.5L×58.5g=29.3g;用固体配制溶液的一般步骤为计算、称量、溶解、转移、洗涤、定容、摇匀可知,④为移液,⑥为定容.
故答案为:29.3;移液;定容;
(2)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶可知所需的仪器有:托盘天平、烧杯、玻璃棒、胶头滴管和500mL容量瓶,故除托盘天平、烧杯、玻璃棒、胶头滴管外,还需500mL容量瓶;容量瓶使用前要查漏;故答案为:500mL容量瓶,查漏;
(3)A.只要定容时正确,至于水是原来就有的还是后来加入的,对浓度无影响,即容量瓶未干燥即用来配制溶液,对溶液浓度无影响,故A错误;
B.溶液从烧杯转移到容量瓶中后没有洗涤烧杯,会导致溶质的损失,则所配溶液的浓度偏低,故B正确;
C.定容时观察液面俯视,则溶液的体积偏小,浓度偏高,故C错误;
D.滴管加水时,有少量水滴到容量瓶外,对溶质的量和溶液体积无影响,则对浓度无影响,故D错误;
E.定容摇匀后,发现液面低于刻度线是正常的,又滴加蒸馏水至刻度则导致浓度偏小,故E正确.
故选BE.
(4)溶液是均一稳定的,取出一部分氯化钠溶液对其浓度无影响,即溶液的浓度仍为1.00mol/L,故答案为:1.00mol/L.
点评 本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,属于基础型题目,难度不大.

| A. | Na2SiO3 | B. | BaCl2 | C. | AgNO3 | D. | NaAlO2 |
| A. | 39g | B. | 59g | C. | 78g | D. | 97g |
| A. | HO-CH2CH2-COOH | B. | HOOC-COOH | C. | HO-CH2CH2-OH | D. | CH2-COOH |
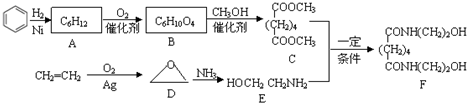

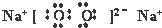 .
.