题目内容
(8分)在室温下,向100mL Cu(IO3)2饱和溶液中加入足量的经硫酸酸化的KI溶液,发生如下反应: 、
、 ,反应完全后,用0.1 mol/L的Na2S2O3溶液滴定,
,反应完全后,用0.1 mol/L的Na2S2O3溶液滴定,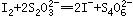 ,消耗了40 mL Na2S2O3溶液,计算:
,消耗了40 mL Na2S2O3溶液,计算:
(1)原饱和溶液中Cu(IO3)2的物质的量浓度;
(2)若Cu(IO3)2饱和溶液的密度为1.0 g/cm3,室温时Cu(IO3)2的溶解度是多少?
 、
、 ,反应完全后,用0.1 mol/L的Na2S2O3溶液滴定,
,反应完全后,用0.1 mol/L的Na2S2O3溶液滴定,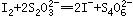 ,消耗了40 mL Na2S2O3溶液,计算:
,消耗了40 mL Na2S2O3溶液,计算:(1)原饱和溶液中Cu(IO3)2的物质的量浓度;
(2)若Cu(IO3)2饱和溶液的密度为1.0 g/cm3,室温时Cu(IO3)2的溶解度是多少?
(1)3.1×10-3 mol/L(2)0.13 g
(1)1Cu(IO3)2 ~ 6.5I2 ~ 13Na2S2O3
1mol 6.5mol 13mol
C [Cu(IO3)2]·0.1L 0.1 mol/L×0.04L
C [Cu(IO3)2]= 3.1×10-3 mol/L
(2)若Cu(IO3)2饱和溶液的密度为1.0 g/cm3,则100mL Cu(IO3)2饱和溶液为100g,其中Cu(IO3)2的质量为3.1×10-3 mol/L×0.1L×414g/mol="0.13" g,则室温时Cu(IO3)2的溶解度近似为0.13 g。
1mol 6.5mol 13mol
C [Cu(IO3)2]·0.1L 0.1 mol/L×0.04L
C [Cu(IO3)2]= 3.1×10-3 mol/L
(2)若Cu(IO3)2饱和溶液的密度为1.0 g/cm3,则100mL Cu(IO3)2饱和溶液为100g,其中Cu(IO3)2的质量为3.1×10-3 mol/L×0.1L×414g/mol="0.13" g,则室温时Cu(IO3)2的溶解度近似为0.13 g。

练习册系列答案
相关题目
 量Fe反应,转移的电子数为3 n。
量Fe反应,转移的电子数为3 n。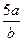 mol/L
mol/L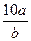 mol/L
mol/L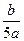 mol/L
mol/L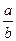 mol/L
mol/L