��Ŀ����
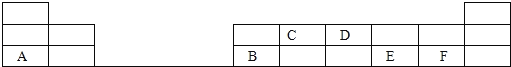
����Ŀ��ijͬѧ��������������������ᷴӦ�й�ʵ�飬ʵ����̵����ݼ�¼���£����������ϱ�����Ϣ���ش��й����⣺

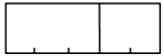
(1)д��������Ӧ�����ӷ���ʽ__________��
(2)�����������յ�֪ʶ�жϣ�������ʵ���з�Ӧ�������Ŀ�����__________����ʵ����ţ���
(3)�����ñȽ�ijһ���ض�ʵ�������Ӱ��ʱ�������ų��������صı䶯���ţ�����Ҫ���ƺ���ʵ���йصĸ��Ӧ���������У�
����˵���¶ȶԸ÷�Ӧ����Ӱ�����ϱȽ���__________������ʵ����ţ�
��A��B��A��C����ϱȽ����о���������__________��
��B��C����ϱȽ����о���������__________��
(4)�̲��������˳��ֻ�ɫ�����Ŀ������ȽϷ�Ӧ���ʵĿ������������Ϊ�β�������ˮ��������λʱ������������Ĵ�С���б�__________��
���𰸡�S2O32��+2H+�TS��+SO2��+H2O D AD ��ͬ�¶�������Ũ�ȶԸ÷�Ӧ���ʵ�Ӱ�� ��ͬ�¶������£��÷�Ӧ���ʸ���̶���ȡ�������ַ�Ӧ���Ũ�� SO2������ˮ���ⶨ����ȷ��ʵ��װ�ýϸ��ӣ�������
��������
(1)����������ԭ��Ӧ����S�����������ˮ��
(2)�¶�Խ�ߣ���Ӧ����Խ�죬Ũ��Խ��Ӧ����Խ�죬�ȱȽ��¶ȣ�
(3)��A��B��ֻ���¶Ȳ�ͬ��
�ڱ���ֻ��Ũ�ȣ�
��B��C�¶���ͬ���ı䷴Ӧ���Ũ�ȣ�
(4)������ˮ��������λʱ����������������ײ��������������������ˮ��
(1)�����������ϡ���ᷴӦ���������ơ����ʡ����������ˮ����Ӧ�����ӷ�Ӧ����ʽΪ��S2O32��+2H+�TS��+SO2��+H2O��
(2)�¶�Խ�ߣ���Ӧ����Խ�죬Ũ��Խ��Ӧ����Խ�죬��������Ի�ѧ��Ӧ���ʵ�Ӱ�죺����>�¶�>Ũ��(��ѹǿ)������������ʵ���з�Ӧ�������Ŀ�����D��
(3)����˵���¶ȶԸ÷�Ӧ����Ӱ�����������ߵ��¶Ȳ�ͬ��������������ͬ����ѡAD��
��A��B��A��C������в�ͬ����������Ũ�ȣ����ԱȽ����о�����������ͬ�¶�������Ũ�ȶԸ÷�Ӧ���ʵ�Ӱ�죻
��B��C����ϲ�ͬ���ǣ���������ƺ������Ũ�Ȳ�ͬ�����ԱȽ����о�����������ͬ�¶������£��÷�Ӧ���ʸ���̶���ȡ�������ַ�Ӧ���Ũ�ȣ�
(4)��������������ˮ��1���ˮ���ܽ�40��������������Ե��²ⶨ����ȷ���Ҹ�ʵ��װ�ýϸ��ӣ������ƣ����Բ�������ˮ��������λʱ������������Ĵ�С���бȽϡ�