题目内容
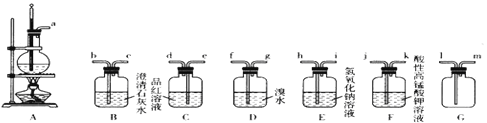
【题目】在1﹣18号的短周期主族元素中,表中的字母代表一种元素,回答下列问题:
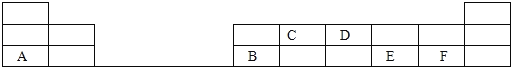
(1)画出D的原子结构示意图________;
(2)写出C的最高价氧化物的电子式________,该化合物所含化学键为____;
(3)E和F分别形成的气态氢化物中最稳定的是____(填写氢化物的化学式);
(4)A最高价氧化物的水化物与B的最高价氧化物的水化物的化学反应方程式____。
【答案】
![]() 共价键 HCl NaOH+Al(OH)3=NaAlO2+2H2O
共价键 HCl NaOH+Al(OH)3=NaAlO2+2H2O
【解析】
根据元素在周期表中的位置,可知A为Na,B为Al,C为C,D为N,E为S,F为Cl。
(1)D为N元素,为7号元素,其原子结构示意图为 ;
;
(2)C为C元素,其最高价氧化物为CO2,C原子最外层4个电子,达到稳定结构,需要形成4对共用电子对,O原子最外层有6个电子,达到稳定结构需要形成2对共用电子对,因此CO2分子中,1个C原子分别和2个O原子形成2对共用电子对,电子式为![]() ,所含化学键为共价键;
,所含化学键为共价键;
(3)同周期非金属元素的非金属性从左到右依次增强,元素的非金属性越强,其气态氢化物的稳定性越强,Cl的非金属性强于S,则HCl稳定;
(4)A的最高价氧化物的水化物为NaOH,B的最高价氧化物的水化物为Al(OH)3;两者反应生成NaAlO2和水,化学方程式为NaOH+Al(OH)3=NaAlO2+2H2O。

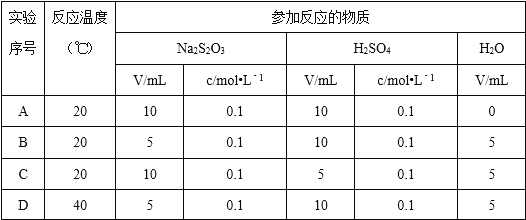
【题目】实验室合成溴苯的装置图及有关数据如下,按下列合成步骤回答:
苯 | 溴 | 溴苯 | |
密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |

(1)实验装置中,仪器c的名称为__________________,作用为__________。
(2)在a中加入15 mL无水苯和少量铁屑,在b中小心加入4.0 mL液态溴,向a中滴入几滴溴,有白雾产生,是因为生成了________气体,继续滴加至液溴滴完。写出a中发生反应的化学方程式:__________________。
(3)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10 mL水,然后过滤除去未反应的铁屑;
②滤液依次用10 mL水、8 mL 10%的NaOH溶液、10 mL水洗涤。NaOH溶液洗涤的作用__________;
③向分出的粗溴苯中加入少量的无水氯化钙(一种干燥剂),静置、过滤。加入无水氯化钙的目的是__________________。
(4)经以上分离操作后,粗溴苯中还含有的主要杂质为______,要进一步提纯,需进行的操作方法为________。