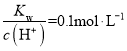题目内容
【题目】下列说法正确的是
A.①2NO2![]() N2O4 ②N2O4
N2O4 ②N2O4![]() 2NO2,反应①的化学平衡常数是反应②的化学平衡常数的倒数
2NO2,反应①的化学平衡常数是反应②的化学平衡常数的倒数
B.已知H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ/mol,将0.05mol/LBa(OH)2溶液100.0mL与0.05mol/LH2SO4溶液100.0mL混合,在298K、101kPa条件下放热量为0.573kJ
C.已知298K 时,0.10mol/L HAc的电离度为1.32%。在0.10mol/L HAc和0.10mol/LNaAc的混合溶液20.00mL中,有如下变化:①HAc![]() H++Ac-,②NaAc=Na++Ac-,③Ac-+H2O
H++Ac-,②NaAc=Na++Ac-,③Ac-+H2O![]() HAc+OH-,向该溶液中滴入几滴稀盐酸,溶液的pH保持相对稳定
HAc+OH-,向该溶液中滴入几滴稀盐酸,溶液的pH保持相对稳定
D.将明矾与纯碱溶液混合,有沉淀产生,该沉淀的成分为碳酸铝
【答案】C
【解析】
A.在相同温度下,反应①的化学平衡常数才是反应②的化学平衡常数的倒数,A项错误;
B.Ba(OH)2和硫酸反应生成水和硫酸钡沉淀,生成硫酸钡沉淀也有热效应,所以将0.05mol/LBa(OH)2溶液100.0mL与0.05mol/LH2SO4溶液100.0mL混合,在298K、101kPa条件下放热量不等于0.573kJ,B项错误;
C.0.10mol/L HAc和0.10mol/LNaAc的混合溶液,相当于缓冲溶液,向该溶液中滴入几滴稀盐酸,HAc![]() H++Ac-,平衡逆向移动,溶液的pH保持相对稳定,C项正确;
H++Ac-,平衡逆向移动,溶液的pH保持相对稳定,C项正确;
D.将明矾与纯碱溶液混合,Al3+与CO32-水解相互促进,生成CO2和Al(OH)3白色沉淀,D项错误;
选C。

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目