题目内容
12.32g SO2 所含的硫原子的物质的量为( )| A. | 0.2 mol | B. | 0.3 mol | C. | 0.4 mol | D. | 0.5 mol |
分析 根据质量和计算公式n=$\frac{m}{M}$计算出32g SO2的物质的量,结合SO2化学式的组成判断所含硫原子物质的量.
解答 解:32gSO2的物质的量n=$\frac{m}{M}$=$\frac{32g}{64g/mol}$=0.5mol,1个SO2中含有1个硫原子,0.5molSO2中含的硫原子的物质的量为0.5mol,
故选D.
点评 本题考查物质的量的相关计算,题目难度不大,本题注意化学式的组成与所含原子物质的量关系.

练习册系列答案
相关题目
20.下列反应是氧化还原且不是四种基本反应类型的是( )
| A. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | B. | NaOH+HCl═NaCl+H2O | ||
| C. | Fe+CuSO4═Cu+FeSO4 | D. | Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$ 2Fe+3CO2 |
7.NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
| A. | 0.1 mol C3H6Cl2中化学键总数为NA | |
| B. | 42 g乙烯中含碳原子数为3 NA | |
| C. | 标准状况下,1L苯完全燃烧生成的气态产物的分子数为$\frac{6}{22.4}$NA | |
| D. | 0.1 mol乙醇完全燃烧所消耗的氧分子数一定为0.3 NA |
17.下列制取单质的反应中,化合物作还原剂的是( )
| A. | Br2+2NaI═2NaBr+I2 | B. | Zn+H2SO4═ZnSO4+H2↑ | ||
| C. | 2C+SiO2$\frac{\underline{\;\;△\;\;}}{\;}$Si+2CO↑ | D. | 4Al+3MnO2 $\frac{\underline{\;\;△\;\;}}{\;}$3Mn+2Al2O3 |
4.下列做法中不能防止钢铁生锈的是( )
| A. | 安置在潮湿环境中 | B. | 涂油漆 | ||
| C. | 镀铬 | D. | 接镁块 |
1.下列物质属于非电解质的是( )
| A. | H2SO4 | B. | Cl2 | C. | CaCO3 | D. | CO2 |
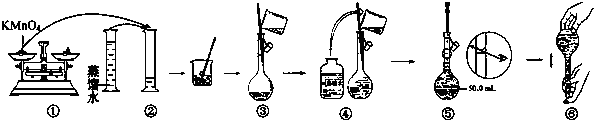
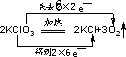 .
.