题目内容
【题目】铅蓄电池的充放电反应为Pb(s)+PbO2(s)+2H2SO4(aq)![]() 2PbSO4(s)+2H2O(1)。某铅蓄电池的正、负极标记被磨损,试用如困装置设计实验,识别出此铅蓄电池的正、负极。
2PbSO4(s)+2H2O(1)。某铅蓄电池的正、负极标记被磨损,试用如困装置设计实验,识别出此铅蓄电池的正、负极。

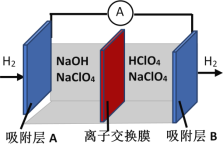
(1)将A接E、B接F,B电极出现_____________现象,电极反应式为_____________,说明F为正极。
(2)铅蓄电池工作时(放电),E电极的反应式为_____________,充电时该极与外接电源的_____________极相连。
(3)若有0.2mol电子发生转移,则正极消耗PbO2的物质的量是______mol。
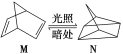
(4)如图是在金属锌板上贴上一张用某溶液浸湿的滤纸。

①若用硫酸钠和酚酞的混合溶液浸湿滤纸,用导线将a、b直接相连,则滤纸出现____色,铅笔芯c点处的电极反应式为________________。
②若用KI-淀粉溶液浸湿滤纸,用导线将a、b与铅蓄电池的E、F电极相连,铅笔芯c点处出现蓝色,则b接的是_______(填“E”或“F”)电极。
【答案】有气泡产生 2Cl--2e- = Cl2↑ Pb(s) - 2e-+ SO42- = PbSO4 负 0.1 红 O2 + 4e-+ 2H2O = 4OH- F
【解析】
(1)F要证明是正极,说明B为阳极。
(2)铅蓄电池工作时(放电),E电极为负极,充电时该极与外接电源的负极相连。
(3)根据方程式分析,1mol PbO2反应转移2mol电子。
(4)①导线将a、b直接相连,则锌板为负极,铅笔为正极,氧气反应生成氢氧根;②若用KI-淀粉溶液浸湿滤纸,铅笔芯c点处出现蓝色,说明c点生成了单质碘,则c为阳极。
(1)F要证明是正极,说明B为阳极,阳极应该阴离子氯离子放电变为氯气,因此B电极出现有气泡产生现象,电极反应式为2Cl--2e- = Cl2↑;故答案为:有气泡产生;2Cl--2e- = Cl2↑。
(2)铅蓄电池工作时(放电),E电极为负极,其负极反应式为Pb(s) - 2e-+ SO42- = PbSO4,充电时该极与外接电源的负极相连;故答案为:Pb(s) - 2e-+ SO42- = PbSO4;负。
(3)根据Pb(s)+PbO2(s)+2H2SO4(aq)![]() 2PbSO4(s)+2H2O(1),1mol PbO2反应转移2mol电子,若有0.2mol电子发生转移,则正极消耗PbO2的物质的量是0.1 mol;故答案为:0.1。
2PbSO4(s)+2H2O(1),1mol PbO2反应转移2mol电子,若有0.2mol电子发生转移,则正极消耗PbO2的物质的量是0.1 mol;故答案为:0.1。
(4)①若用硫酸钠和酚酞的混合溶液浸湿滤纸,用导线将a、b直接相连,则锌板为负极,铅笔为正极,氧气反应生成氢氧根,氢氧根使酚酞变红,因此滤纸出现红色,铅笔芯c点处的电极反应式为O2 + 4e-+ 2H2O = 4OH-;故答案为:红;O2 + 4e-+ 2H2O = 4OH-。
②若用KI-淀粉溶液浸湿滤纸,铅笔芯c点处出现蓝色,说明c点生成了单质碘,则c为阳极,连接电源正极,则b接的是正极即F电极;故答案为:F。

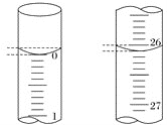
【题目】某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液,若滴定开始和结束时,酸式滴定管中的液面如图所示:

(1)所用盐酸溶液的体积为________mL
(2)用标准的盐酸溶液滴定待测的氢氧化钠溶液时,用酚酞做指示剂,达到滴定终点的现象是:_____
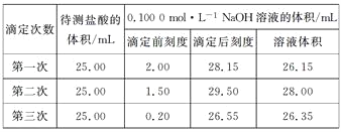
(3)某学生根据三次实验分别记录有关数据如下表:
滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000molL-1盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
请选用其中合理数据列出该氢氧化钠溶液物质的量浓度(计算结果保留4位有效数字):c(NaOH)=_______
(4)由于错误操作,使得上述所测氢氧化钠溶液的浓度偏高的是_______(填写编号)。
A.中和滴定达终点时俯视滴定管内液面读数。
B.碱式滴定管用蒸馏水洗净后立即取用25.00mL待测碱溶液注入锥形瓶进行滴定。
C.酸式滴定管用蒸馏水洗净后立即装标准溶液来滴定。
D.把配好的标准溶液倒入刚用蒸馏水洗净的试剂瓶中然后用来滴定。
【题目】下表是元素周期表的一部分,其中每个数字序号代表一种短周期元素。
| IA | 0 | |||||||
1 | ① | II A | III A | IV A | V A | VI A | VIIA | ||
2 | ② | ③ | |||||||
3 | ④ | ⑤ | ⑥ | ||||||
请按要求回答下列问题:
(1)元素③的最高价氧化物对应的水化物的化学式为 ;
(2)②、③两元素的原子半径较大的是______________(填元素符号);
(3)④和⑤两种元素的金属性较强的是 (填元素符号);
(4)元素③和元素⑥的氢化物均极易溶于水,用两根玻璃棒分别蘸取它们的浓溶液,相互接近时,可看到大量的白烟,写出产生该现象的化学方程式 。