题目内容
10.下列说法正确的是(NA为阿伏加德罗常数)( )| A. | 124 g P4含有P-P键的个数为4NA | |
| B. | 12 g石墨中含有C-C键的个数为1.5NA | |
| C. | 12 g金刚石中含有C-C键的个数为4NA | |
| D. | 60gSiO2中含Si-O键的个数为2NA |
分析 通过n=$\frac{m}{M}$计算各物质的物质的量,结合各晶体的结构确定各个化学键的个数.
解答 解:A、n(P4)=$\frac{124g}{124g/mol}$=1mol,1个P4分子含有6个P-P键,因此124g P4含有的P-P键的物质的量为6mol,P-P键的个数为6NA,故A错误;
B、12g石墨中含有碳原子的物质的量n=$\frac{m}{M}$=$\frac{12g}{12g/mol}$=1mol,在石墨晶体中一个碳原子形成3个C-C键,每个C-C键由2个碳原子构成,因此12g石墨中含有C-C键的物质的量为1mol×3×$\frac{1}{2}$=1.5mol,C-C键的个数为1.5NA,故B正确;
C、12g金刚石中含有碳原子的物质的量n=$\frac{m}{M}$=$\frac{12g}{12g/mol}$=1mol,在金刚石晶体中每个碳原子形成4个C-C键,每个C-C键由2个碳原子构成,因此12g金刚石中含有C-C键的物质的量为1mol×4×$\frac{1}{2}$=2mol,C-C键的个数为2NA,故C错误;
D、n( SiO2)=$\frac{m}{M}$=$\frac{60g}{60g/mol}$=1mol,在二氧化硅晶体中,每个硅原子形成4个Si-O键,因此60g SiO2中含Si-O键的物质的量为4mol,Si-O键的个数为4NA,故D错误;
故选B.
点评 本题考查阿伏伽德罗常数的有关计算,难度中等,侧重于分子晶体、原子晶体、混合晶体结构的考查,掌握物质的晶体结构是解题的关键.

练习册系列答案
相关题目
20.下列关于原电池说法正确的是( )
| A. | 原电池是一种直接把化学能转化为电能的装置,在此转化过程中无能量损耗 | |
| B. | 在Zn-Cu-H2SO4构成的原电池中,H+不断移向负极 | |
| C. | 钢铁在潮湿的环境中易被腐蚀与原电池有关 | |
| D. | 纯铁比生铁(含有少量杂质)与稀HCl反应快 |
1.下列说法中,正确的是( )
| A. | 热化学方程式中的化学计量数表示物质的量,可以是分数 | |
| B. | △H>0 kJ•mol-1表示放热反应,△H<0 kJ•mol-1表示吸热反应 | |
| C. | 1 mol H2SO4与1 molBa(OH)2反应生成H2O时放出的热叫做中和热 | |
| D. | 1 mol H2与0.5 molO2反应放出的热就是H2的燃烧热 |
18.某有机化合物的结构简式如图所示,下列叙述不正确的是( )


| A. | 它有酸性,能与纯碱溶液反应 | |
| B. | 它在一定条件下能发生水解,且产物只有一种 | |
| C. | 1 mol该有机物最多能与7 mol NaOH反应 | |
| D. | 1 mol该有机物最多能与4 mol Br2反应 |
2.漂白粉的有效成分是( )
| A. | NaOH | B. | Ca(ClO)2 | C. | NaCl | D. | Na2O2 |
19.下列说法正确的是( )
| A. | 共价化合物中不可能含有离子键 | |
| B. | 只有金属元素和非金属元素才能形成离子键 | |
| C. | 水分子很稳定,因为水分子间存在氢键 | |
| D. | 所有的分子晶体内都存在两种以上作用力 |
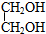 ,写出有关反应的化学方程式.CH3CH2Cl+NaOH$→_{△}^{乙醇}$CH2=CH2+NaCl+H2O;CH2=CH2+Cl2→CH2Cl-CH2Cl;CH2Cl-CH2Cl+2NaOH $→_{△}^{水}$HOCH2CH2OH+2NaCl.
,写出有关反应的化学方程式.CH3CH2Cl+NaOH$→_{△}^{乙醇}$CH2=CH2+NaCl+H2O;CH2=CH2+Cl2→CH2Cl-CH2Cl;CH2Cl-CH2Cl+2NaOH $→_{△}^{水}$HOCH2CH2OH+2NaCl. 1
1