��Ŀ����
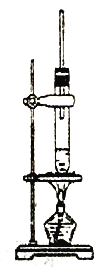
����Ŀ�����ü�������������ȡ����Ӧ��ȡ����Ʒ����������ѳ�Ϊ��ʵ��ij��ѧ��ȤС����ʵ������ģ���������̣���Ӧ������������ը��������Ƶ�ģ��װ�����£�

����Ҫ����գ�
��1������F������______________��A�з�Ӧ�����ӷ�Ӧ����ʽ___________________��
��2��Bװ�������ֹ��ܣ��ٿ��������ٶȣ��ھ��Ȼ�������______________________��
��3��Ϊ�˳������������Dװ���е�ʯ�������ȸ���KI��ĩ������Ϊ�ܷɼ�ʯ��______����ܡ����ܡ�����
��4��Eװ�õ�����________��
A.�ռ����� B.�������� C.��ֹ���� D.�����Ȼ���
��5��Eװ���г�������������,�������л���,��E�з�����������ѷ�����_____________________________��
���𰸡���Һ©��MnO2+4H++2Cl![]() Mn2++Cl2��+2H2O������鲻�ܣ����ɵ�HCl�ᱻ��ʯ������C��D��Һ
Mn2++Cl2��+2H2O������鲻�ܣ����ɵ�HCl�ᱻ��ʯ������C��D��Һ
��������
�ڼ��������£�Ũ����Ͷ������̷�Ӧ����������Ũ���������ˮ�ԣ��������������C�м���������ڹ��������·���ȡ����Ӧ�����ȴ�����HCl��D��ʯ����KI���⻯�غ�������Ӧ���ɵ���Ȼ��ƣ�β���к����Ȼ��⣬�Ȼ��⼫������ˮ������Eװ���������Ȼ��⣬���۵�©���ܷ��������ݴ˽��
��1������F������Ϊ��Һ©�������������£�Ũ����Ͷ������̷�Ӧ������������Ӧ�����ӷ���ʽΪMnO2+4H++2Cl![]() Mn2++Cl2��+2H2O��
Mn2++Cl2��+2H2O��
��2��Ũ���������ˮ�ԣ�����Bװ�õĹ��ܳ����������ٶ������Ȼ����������и����������á�
��3���������ɵ�HCl�ᱻ��ʯ�����գ�����Dװ���е�KI��ĩ���ܻ��ɼ�ʯ����
��4��E�������Ȼ������ܷ�ֹ����������Eװ�������������Ȼ���ͷ�ֹ������������ѡCD��
��5���ȴ�����������ˮ����HCl��������ˮ�����Բ��÷�Һ���������ᴿ��

����Ŀ��һ���¶��£����ܱ�������X��Y��Z��W��������ij�ʼŨ�Ⱥ�ƽ��Ũ�������ʾ������˵������ȷ����
���� | X | Y | Z | W |
��ʼŨ��/mol��L��1 | 0.5 | 0.5 | 0 | 0 |
ƽ��Ũ��/mol��L��1 | 0.1 | 0.1 | 0.4 | 0.4 |
A. ��Ӧ�ﵽƽ��ʱ��X���������Ϊ10%
B. ���¶��·�Ӧ��ƽ�ⳣ��K��16
C. �����¶Ȳ�������ѹǿ����Ӧ���ʼӿ죬ƽ��������Ӧ�����ƶ�
D. ��X��Y�ij�ʼŨ�Ⱦ�Ϊ0.8 mol��L��1����ﵽƽ��ʱ��W��Ũ��Ϊ0.64 mol��L��1