题目内容
16.写出下列物质电离方程式:①NaCl:NaCl=Na++Cl-
②Fe2(SO4)3:Fe2(SO4)3=2Fe3++3SO42-.
分析 ①氯化钠属于强电解质,完全电离;
②硫酸铁属于强电解质,完全电离;
解答 解:①氯化钠属于强电解质,完全电离,电离方程式:NaCl=Na++Cl-,故答案:NaCl=Na++Cl-;
②硫酸铁属于强电解质,完全电离,电离方程式:Fe2(SO4)3=2Fe3++3SO42-故答案:Fe2(SO4)3=2Fe3++3SO42-.
点评 本题考查了电解质电离方程式的书写,明确电解质强弱及电离方式是解题关键,注意弱电解质部分电离用可逆号,强电解质完全电离,用等号,题目难度不大.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
7.下列混合物可采用蒸馏法分离的一组是( )
| A. | 水与四氯化碳 | B. | 食盐与泥沙 | C. | 硝酸钾与氯化钾 | D. | 溴与四氯化碳 |
4.若NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 在0℃、101 kPa时,22.4L氢气中含有NA个氢原子 | |
| B. | NA个CO分子和0.5mol CH4的质量比为7:4 | |
| C. | 16gCH4与18gNH${\;}_{4}^{+}$所含质子数相等 | |
| D. | 常温常压下,92g的NO2和N2O4混合气体中含有的原子数为6NA |
3.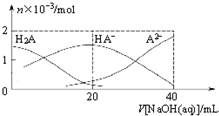 25℃下,向20mL 0.1mol•L-1H2A溶液中滴加0.1mol•L-1NaOH溶液,有关粒子物质的量的变化如图所示.下列有关说法正确的是( )
25℃下,向20mL 0.1mol•L-1H2A溶液中滴加0.1mol•L-1NaOH溶液,有关粒子物质的量的变化如图所示.下列有关说法正确的是( )
 25℃下,向20mL 0.1mol•L-1H2A溶液中滴加0.1mol•L-1NaOH溶液,有关粒子物质的量的变化如图所示.下列有关说法正确的是( )
25℃下,向20mL 0.1mol•L-1H2A溶液中滴加0.1mol•L-1NaOH溶液,有关粒子物质的量的变化如图所示.下列有关说法正确的是( )| A. | H2A属于强酸 | |
| B. | $\frac{c(H{A}^{-})}{c({H}_{2}{A}^{\;})}$随着V[NaOH(aq)]的增大而减小 | |
| C. | V[NaOH(aq)]=20mL时,溶液中存在关系:c(HA-)+c(A2-)+c(H2A)=0.1mol•L-1 | |
| D. | V[NaOH(aq)]=20mL时,溶液中存在关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
4.下列各组物质中,各成分都属于电解质的是( )
| A. | 磷酸晶体和磷酸溶液 | B. | 硝酸钾晶体和熔化的硝酸钾 | ||
| C. | 蔗糖晶体和熔化的蔗糖 | D. | 熟石灰和澄清石灰水 |