题目内容
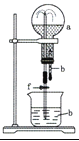
【题目】甲、乙、丙三位同学分别用如下三套实验装置及化学药品(其中碱石灰为固体氢氧化钠和生石灰的混合物)制取氨气。请你回答下列问题:
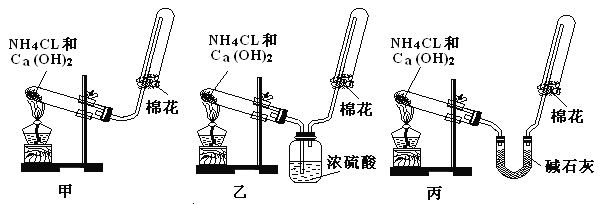
(1)三位同学制取氨气的化学方程式为:___________________。
(2)三位同学都用向下排空气法收集氨气,其原因是_____________________。
(3)三位同学用上述装置制取氨气时,其中有一位同学没有收集到氨(如果他们的实验操作都正确),你认为没有收集到氨气的同学是_______ 填(“甲”、“乙”或“丙”),收集不到氨气的主要原因是_________________(用化学方程式表示)。
(4)检验氨气是否收集满的方法是(简述操作方法、现象和结论)__________________。
(5)三位同学都认为他们的实验装置也可用于加热碳酸氢铵固体制取纯净的氨气,你判断能够达到实验目的的是_______ (填“甲”、“乙”或“丙”),该装置中的NH4HCO3固体能否用NH4Cl固体代替?_______ (填“能”或“不能”)。
【答案】 2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O 氨气的密度比空气小 乙 2NH3+H2SO4=(NH4)2SO4 将湿润的红色石蕊试纸靠近试管口,若试纸变蓝,说明已收集满;(或将蘸有浓盐酸的玻璃棒靠近试管口,若有白烟产生,说明已收集满) 丙 不能
CaCl2+2NH3↑+2H2O 氨气的密度比空气小 乙 2NH3+H2SO4=(NH4)2SO4 将湿润的红色石蕊试纸靠近试管口,若试纸变蓝,说明已收集满;(或将蘸有浓盐酸的玻璃棒靠近试管口,若有白烟产生,说明已收集满) 丙 不能
【解析】(1)实验室用氢氧化钙和氯化铵在加热条件下制备氨气,反应方程式为2NH4Cl+Ca(OH)2 ![]() CaCl2+2H2O+2NH3↑;(2)氨气易溶于水,不能用排水法收集,氨气密度比空气小,应用向下排空法收集;(3)氨气为碱性气体,通过盛有浓硫酸的洗气瓶时,与硫酸反应而被吸收,因此装置乙不能收集到氨气,反应方程式为:2NH3+H2SO4=(NH4)2SO4;(4)氨气为碱性气体,与水反应生成NH3H2O,电离子出OH-离子,溶液呈碱性,检验时可用用蘸有浓盐酸的玻璃棒靠近试管口,如果产生白烟,则氨气已满,或用湿润的红色石蕊试纸靠近试管口,如果试纸变蓝,则氨气已满;(5)碳酸氢铵受热分解生成氨气、水和二氧化碳.甲收集到的是混合气体,得不到纯净氨气,乙分解得到二氧化碳、氨气和水蒸气通过浓硫酸氨气被吸收得不到氨气,丙分解得到二氧化碳、氨气和水蒸气,通过碱石灰,吸收二氧化碳和水蒸气得到纯净干燥的氨气,该装置中的NH4HCO3固体不能用NH4Cl固体代替NH3 ,氯化铵分解生成的氨气和氯化氢在试管口处会重新反应生成氯化铵。
CaCl2+2H2O+2NH3↑;(2)氨气易溶于水,不能用排水法收集,氨气密度比空气小,应用向下排空法收集;(3)氨气为碱性气体,通过盛有浓硫酸的洗气瓶时,与硫酸反应而被吸收,因此装置乙不能收集到氨气,反应方程式为:2NH3+H2SO4=(NH4)2SO4;(4)氨气为碱性气体,与水反应生成NH3H2O,电离子出OH-离子,溶液呈碱性,检验时可用用蘸有浓盐酸的玻璃棒靠近试管口,如果产生白烟,则氨气已满,或用湿润的红色石蕊试纸靠近试管口,如果试纸变蓝,则氨气已满;(5)碳酸氢铵受热分解生成氨气、水和二氧化碳.甲收集到的是混合气体,得不到纯净氨气,乙分解得到二氧化碳、氨气和水蒸气通过浓硫酸氨气被吸收得不到氨气,丙分解得到二氧化碳、氨气和水蒸气,通过碱石灰,吸收二氧化碳和水蒸气得到纯净干燥的氨气,该装置中的NH4HCO3固体不能用NH4Cl固体代替NH3 ,氯化铵分解生成的氨气和氯化氢在试管口处会重新反应生成氯化铵。