题目内容
【题目】色氨酸是植物体内生长素生物合成重要的前体物质,普遍存在于高等植物中.纯净的色氨酸为白色或微黄色结晶,微溶于水易溶于盐酸或氢氧化钠,其结构如图所示,下列关于色氨酸的说法不正确的是( ) 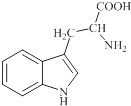
A.色氨酸的分子式为C11H12N2O2
B.色氨酸能发生取代、加成、酯化、中和反应
C.色氨酸微溶于水而易溶于酸或碱溶液是因为其与酸、碱都能反应生成盐
D.将色氨酸与甘氨酸(NH2CH2COOH)混合,在一定条件下最多可形成三种二肽
【答案】D
【解析】解:A.根据结构简式知,色氨酸的分子式为C11H12N2O2 , 故A正确;
B.色氨酸中含有碳碳双键、氨基、羧基和苯环,具有烯烃、氨基酸和苯的性质,能发生加成反应、氧化反应、缩聚反应、加聚反应、还原反应、酯化反应、中和反应,故B正确;
C.色氨酸中含有羧基和氨基,能和碱、酸反应生成盐,烃基相对分子质量较大,烃基对其溶解度影响较大,所以微溶于水,故C正确;
D.色氨酸分子中含有两个氨基一个羧基,甘氨酸中含有一个羧基和一个氨基,色氨酸自身能形成两种二肽、甘氨酸自身能形成一种二肽,色氨酸与甘氨酸(NH2CH2COOH)能形成三种二肽,所以一共能形成6种二肽,故D错误;
故选D.
【考点精析】通过灵活运用有机物的结构和性质,掌握有机物的性质特点:难溶于水,易溶于汽油、酒精、苯等有机溶剂;多为非电解质,不易导电;多数熔沸点较低;多数易燃烧,易分解即可以解答此题.

【题目】A、B、C、D、E是元素周期表中前四周期中五种常见元素,其相关信息如表:
元素 | 相关信息 |
A | 原子核外L层电子数是K层的2倍 |
B | 其一种单质被称为地球生物的“保护伞” |
C | 元素的第一电离能是第3周期所有元素中最小的 |
D | 基态原子最外层电子排布为(n+1)sn(n+1)p(n+2) |
E | 可形成多种氧化物,其中一种为具有磁性的黑色晶体 |
请回答下列问题:
(1)C在元素周期表中位于第周期、第族;D的基态原子核外电子排布式是 .
(2)B、C、D的简单离子半径由大到小的顺序为(用化学符号表示,下同) , B、D的简单氢化物中稳定性较大的是 .
(3)B的常见单质和C的单质按物质的量比1:2反应生成的化合物中化学键的类型为;该化合物属于晶体.
(4)E形成的黑色磁性晶体发生铝热反应的化学方程式是 .
(5)已知:2AB(g)+B2(g)═2AB2(g)△H=﹣566.0kJmol﹣1
D(s)+B2(g)═DB2(g)△H=﹣296.0kJmol﹣1
处理含AB、DB2烟道气污染的一种方法是将其在催化剂作用下转化为固态单质D,请写出此反应的热化学方程式: .