��Ŀ����
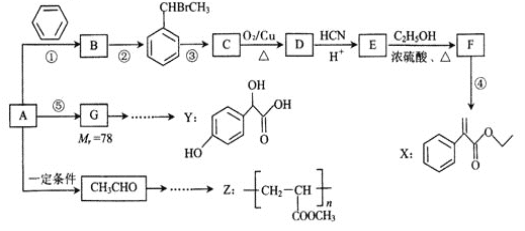
����Ŀ��������̼�Ļ��������ǻ��������о����ȵ���⡣
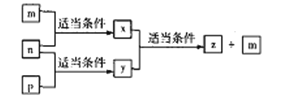
��1����̫���ܵ������£���CO2Ϊԭ����ȡ̿�ڵ�������ͼ1��ʾ�����ܷ�Ӧ�Ļ�ѧ����ʽΪ_________��

��2��CO2�������⻯�ϳɵ�̼ϩ������ϳ���ϩ�ķ�ӦΪ2CO2��g��+6H2��g��![]() CH2=CH2��g��+4H2O��g����H���������ʵ��������ڱ�״���£��涨���ʵ�����Ϊ0�������������������ʱ���ų������յ����������±���ʾ��
CH2=CH2��g��+4H2O��g����H���������ʵ��������ڱ�״���£��涨���ʵ�����Ϊ0�������������������ʱ���ų������յ����������±���ʾ��
���� | H2��g�� | CO2��g�� | CH2=CH2��g�� | H2O��g�� |
����/kJmol-1 | 0 | -394 | 52 | -242 |
���H=_________��
��3����2L�����ܱ������г���2molCO2��nmolH2����һ�������·�����2���еķ�Ӧ��CO2��ת�������¶ȡ�Ͷ�ϱ�[X= ![]() ]�Ĺ�ϵ��ͼ2��ʾ��
]�Ĺ�ϵ��ͼ2��ʾ��
��X1_________X2�����������������=������ͬ����ƽ�ⳣ��KA_________KB��
����B���Ͷ�ϱ�Ϊ3���Ҵӷ�Ӧ��ʼ��B����Ҫ10min����v��H2��=_________��
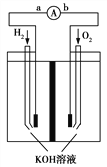
��4����ϡ����Ϊ�������Һ������̫���ܽ�CO2ת��Ϊ��̼ϩ��������ԭ��ͼ��ͼ3��
��b�缫��������_________��
�ڲ�����ϩ�ĵ缫��ӦʽΪ_______________��
���𰸡� ![]()
![]()
![]()
![]()
![]()
![]()
![]()
����������1����700K�����£�CO2��FeO������Ӧ����C��Fe3O4������1��Fe3O4�ֽ�����FeO��O2������������Ӧ������FeO�����������ݷ�Ӧ��������P��Ӧ������д����ʽΪCO2![]() C+O2���ʴ�Ϊ��CO2
C+O2���ʴ�Ϊ��CO2![]() C+O2��
C+O2��
��2���ʱ������������������ȥ��Ӧ������������÷�Ӧ���ʱ�=[52+��-242����4-��-392����2-0]kJ/mol=-128kJ/mol���ʴ�Ϊ��-128kJ/mol��
��3������ͬ�����£�Ͷ�ϱ�[X=![]() ]Խ������̼��ת����Խ����ͼ֪����ͬ�¶���X1��ת���ʴ���X2������X1��X2���÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ���¶�Խ����ƽ�ⳣ��ԽС���¶�A��B������ƽ�ⳣ��A��B���ʴ�Ϊ����������
]Խ������̼��ת����Խ����ͼ֪����ͬ�¶���X1��ת���ʴ���X2������X1��X2���÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ���¶�Խ����ƽ�ⳣ��ԽС���¶�A��B������ƽ�ⳣ��A��B���ʴ�Ϊ����������
����B���Ͷ�ϱ�Ϊ3���Ҵӷ�Ӧ��ʼ��B����Ҫ10min��n��CO2��=2mol����n��H2��=10mol��B�������̼��ת����Ϊ75%����μӷ�Ӧ��n��CO2��=2mol��75%=1.5mol�����ݶ�����̼������֮��Ĺ�ϵʽ֪���μӷ�Ӧ��n��H2��=3n��CO2��=4.5mol����v��H2��=![]() =
=![]() =0.225mol/��L��min�����ʴ�Ϊ��0.225mol/��L��min����
=0.225mol/��L��min�����ʴ�Ϊ��0.225mol/��L��min����
��4��������ͼ֪�����������ĵ缫�������������������ĵ�Դ�缫Ϊ����������bΪ�������ʴ�Ϊ��������
�������϶�����̼�õ��Ӻ������ӷ�Ӧ���ɱ�ϩ��ˮ���缫��ӦʽΪ3CO2+18H++18e-��CH3CH=CH2+6H2O���ʴ�Ϊ��3CO2+18H++18e-��CH3CH=CH2+6H2O��