题目内容
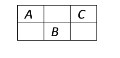
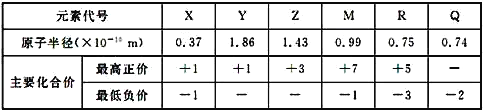
【题目】几种短周期元素的原子半径及主要化合价如下表,下列说法正确的是
A. 离子半径:Y>Z>M
B. Y、Z、M三种元素的最高价氧化物的水化物两两之间会反应
C. 化合物XM、YM都是电解质.熔融状态下都能导电
D. 气态氢化物稳定性R>Q
【答案】B
【解析】
短周期元素,由元素的化合价可知,Q只有最低价-2价,则Q为O元素;M元素有最高价+7,最低-1,故M为Cl;R有+5、-3价,处于ⅤA族,原子半径小于Cl,且与O元素相近,与氧元素同周期,故R为N元素;Z的最高化合价为+3,没有负化合价,处于ⅢA族,且原子半径Z>Cl,处于第三周期,故Z为Al,X、Y均有最高正价+1,处于IA则,而X有-1价,则X为H元素,Y的原子半径比Al的大很多,可知Y为Na;
A.电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越大,故离子半径Cl->Na+>Al3+,故A错误;
B.Y、Z、R的最高价氧化物的水化物分别为氢氧化钠、氢氧化铝、高氯酸,两两之间可以相互反应,故B正确;
C.化合物XM、YM分别为HCl、NaCl,都是电解质,HCl属于共价化合物,熔融状态下不能导电,故C错误;
D.R为N元素,Q为O元素,气态氢化物稳定性NH3<H2O,故D错误;
答案:B。

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目