题目内容
11.某化学兴趣小组欲除去粗盐中可溶性杂质CaCl2、MgCl2、Na2SO4,他们先将粗盐溶于水,然后依次加入过量BaCl2溶液、NaOH溶液、Na2CO3溶液,过滤后加适量稀盐酸,最后经过蒸发操作,就得到了纯净的NaCl固体.分析 从电离的角度分析粗盐中的杂质可知:溶液中的杂质离子为钙离子、镁离子、和硫酸根离子,根据镁离子用氢氧根离子沉淀,硫酸根离子用钡离子沉淀,钙离子用碳酸根离子沉淀,过滤要放在所有的沉淀操作之后,加碳酸钠要放在加氯化钡之后,可以将过量的钡离子沉淀最后再用盐酸处理溶液中的碳酸根离子和氢氧根离子进行分析.
解答 解:首先要把粗盐溶于水形成溶液,然后镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可以将镁离子沉淀,硫酸根离子用钡离子沉淀,加入过量的氯化钡可以将硫酸根离子沉淀,至于先除镁离子,还是先除硫酸根离子都行,钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,Ca2++CO32-=CaCO3↓,但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,Ba2++CO32-=BaCO3↓,离子都沉淀了,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,最后经蒸发操作得到较纯净的氯化钠,
故答案为:BaCl2;盐酸;蒸发.
点评 本题考查了除杂问题,这是化学实验中的一类重要问题,除杂时不仅要能把杂质除掉,还不能引入新杂质,而且方法要简便易行,把握好此原则需要我们有扎实的基础知识和缜密的思维,题目较简单.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.下列反应中属于吸热反应的是( )
| A. | 煅烧石灰石制生石灰 | B. | 燃烧木炭取暖 | ||
| C. | 硝酸与氢氧化钾反应 | D. | 钠与水反应制取氢气 |
2.不能证明苯分子真实结构的事实是( )
| A. | 苯不能使酸性高锰酸钾溶液褪色 | B. | 苯的邻位二溴代物只有一种 | ||
| C. | 苯与溴水混合发生萃取而不加成 | D. | 苯的间位二溴代物只有一种 |
19.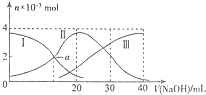 常温下,向20mL0.2mol•L-1H2C2O4溶液中滴加0.2mol•L-1NaOH溶液.有关微粒物质的量的变化如图(其中I代表H2C2O4,Ⅱ代表HC2O4-,Ⅲ代表C2O42-),根据图示判断,下列说法正确的是( )
常温下,向20mL0.2mol•L-1H2C2O4溶液中滴加0.2mol•L-1NaOH溶液.有关微粒物质的量的变化如图(其中I代表H2C2O4,Ⅱ代表HC2O4-,Ⅲ代表C2O42-),根据图示判断,下列说法正确的是( )
 常温下,向20mL0.2mol•L-1H2C2O4溶液中滴加0.2mol•L-1NaOH溶液.有关微粒物质的量的变化如图(其中I代表H2C2O4,Ⅱ代表HC2O4-,Ⅲ代表C2O42-),根据图示判断,下列说法正确的是( )
常温下,向20mL0.2mol•L-1H2C2O4溶液中滴加0.2mol•L-1NaOH溶液.有关微粒物质的量的变化如图(其中I代表H2C2O4,Ⅱ代表HC2O4-,Ⅲ代表C2O42-),根据图示判断,下列说法正确的是( )| A. | H2C2O4在水中的电离方程式是:H2C2O4?2H++C2O42- | |
| B. | 当V(NaOH)=20mL时,溶液中水的电离程度比纯水小 | |
| C. | 当V(NaOH)=30mL时,溶液中存在以下关系:2c(H+)+2c(HC2O4-)+3c(H2C2O4)═c(C2O42-)+2c(OH-) | |
| D. | 已知H2C2O4的电离常数分别为K1、K2,则a点的c(H+)=K2 |
6.某烃分子中有一个环状结构和两个双键,它的分子式可能是( )
| A. | C4H6 | B. | C7H8 | C. | C5H6 | D. | C10H14 |
16.如表实验“操作和现象”与“结论”对应关系正确的是( )
| 选项 | 实验操作及现象 | 实验结论 |
| A | 用铂丝做某溶液的焰色反应,火焰呈黄色 | 该溶液中一定含有钠盐 |
| B | 将二氧化硫通入到溴水中,溴水褪色 | 二氧化硫具有漂白性 |
| C | 在滴有酚酞的Na2CO3溶液中,滴加入BaC12溶液,溶液红色逐渐褪去. | Na2CO3溶液中存在水解平衡 |
| D | 某钾盐溶于盐酸,产生能使澄清石灰水变浑浊的无色无味气体 | 该钾盐是K2CO3 |
| A. | A | B. | B | C. | C | D. | D |
3.下列说法正确的是( )
| A. | 有机物CH2=CH-CH3中碳原子的杂化类型有sp3 和sp2,其中有两个π键,7个σ键 | |
| B. | 分子CO和N2的原子总数相同,价电子总数相等,化学性质相似 | |
| C. | Na+的电子排布式为1s22s22p63s1 | |
| D. | 原子由激发态向基态跃迁时通常以光的形式释放能量 |
20.关于实验室制取乙炔,下列描述合理的是( )
| A. | 乙炔气体中常含有杂质,通常采用硫酸铜溶液洗气除杂 | |
| B. | 为了加快此反应的反应速率,通常往水中加入少许盐酸 | |
| C. | 将生成的气体直接通往溴水中,溴水褪色则证明产生了乙炔 | |
| D. | 通常采取向上排空气法收集乙炔 |
1.课本实验中出现的“草酸溶液与酸性高锰酸钾溶液反应,其反应速率逐渐加快”.经分析某粒子具有催化作用,该粒子是( )
| A. | H+ | B. | SO42- | C. | MnO4- | D. | Mn2+ |